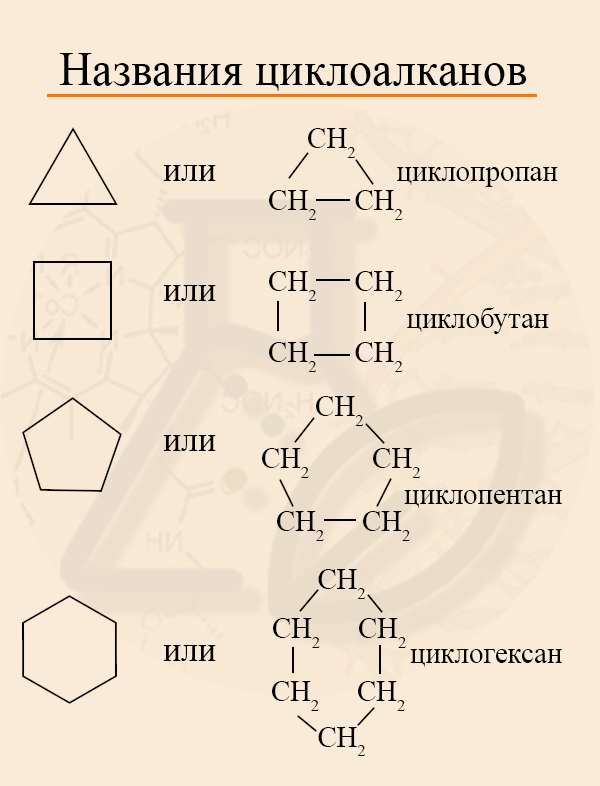
Циклоалканы – это предельные (насыщенные) углеводороды, которые содержат замкнутый углеродный цикл.
Общая формула циклоалканов CnH2n, где n≥3.
Строение, номенклатура и изомерия циклоалканов
Химические свойства циклоалканов
Получение циклоалканов
Строение циклоалканов
Атомы углерода в молекулах циклоалканов находятся в состоянии sp3-гибридизации и образует четыре σ-связи С–С и С–Н. В зависимости от размеров цикла меняются валентные углы.
В малых циклах (циклопропан и циклобутан) валентные углы между связями С–С сильно отличаются от валентных углов между связями С–С в алканах (109о35′). Поэтому в малых циклах возникает напряжение, которое приводит к высокой реакционной способности таких циклоалканов.
Самый простой циклоалкан — циклопропан, представляет, по сути, плоский треугольник.
σ-Связи в циклопропане называют «банановыми». Они не лежат вдоль оси, соединяющей ядра атомов, а отклоняются от неё, уменьшая напряжение в молекуле циклопропана.
По свойствам «банановые» связи напоминают π-связи. Они легко разрываются.
Поэтому циклопропан очень легко вступает в реакции присоединения с разрывом углеродного цикла.
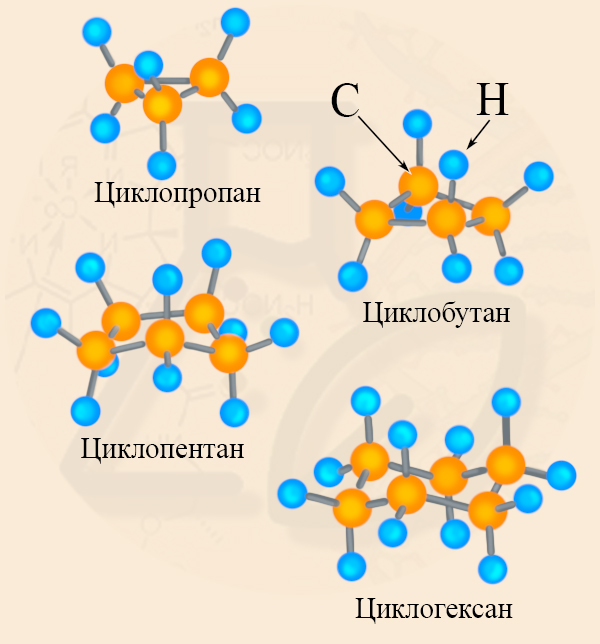
Остальные циклоалканы имеют неплоское строение. Молекула циклобутана имеет перегиб по линии, соединяющей первый и третий атомы углерода в кольце:
Циклобутан также вступает в реакции присоединения, но угловое напряжение в циклобутане меньше, чем в циклопропане, поэтому реакции присоединения к циклобутану протекают сложнее.
Большие циклы имеют более сложное, неплоское строение, вследствие чего угловое напряжение в молекулах больших циклоалканов почти отсутствует.
Циклоалканы с большим циклом не вступают в реакции присоединения. Для них характерны реакции замещения.
Строение циклопентана также неплоское, молекула представляет собой так называемый «конверт».
Молекула циклогексана не является плоским многоугольником и принимает различные конформации, имеющие названия «кресло» и «ванна»:
«кресло» «ванна»
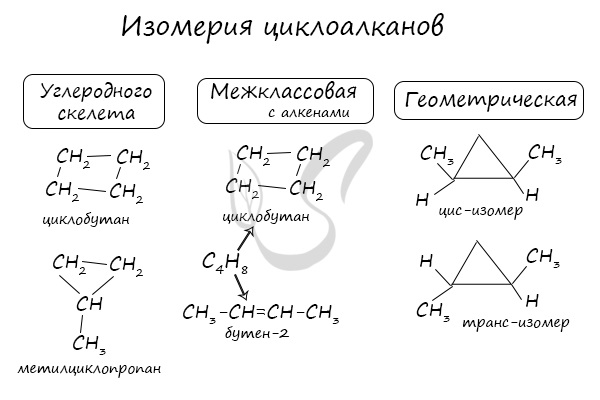
Изомерия циклоалканов
Структурная изомерия
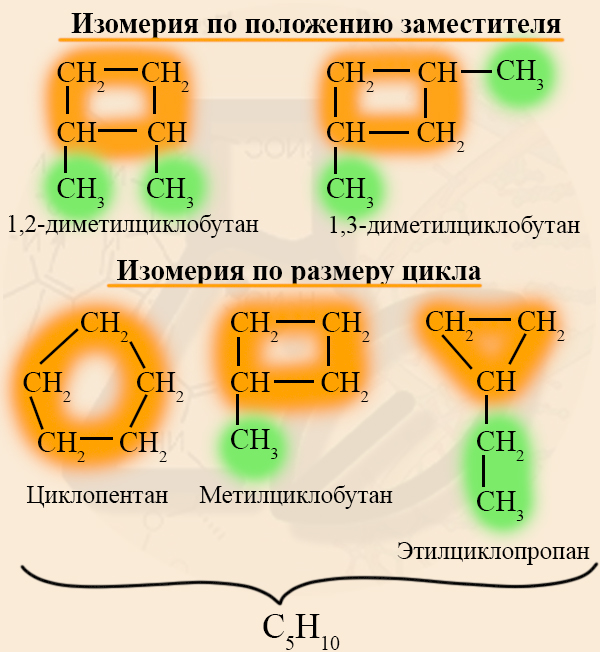
Для циклоалканов характерна структурная изомерия, связанная с разным числом углеродных атомов в кольце, разным числом углеродных атомов в заместителях и с положением заместителей в цикле.
- Изомеры с разным числом атомов углерода в цикле отличаются размерами углеродного цикла.
Изомеры с разным числом углеродных атомов в цикле – это этилциклопропан и метилциклобутан с общей формулой С5Н10
- Изомеры с разным числом атомов углерода в заместителях отличаются строением заместителей у одинакового углеродного цикла.
Структурные изомеры с различным числом углеродных атомов в заместителях – 1-метил-2-пропилциклопентан и 1,2-диэтилциклопентан
- Изомеры с разным положением одинаковых заместителей в углеродном цикле.
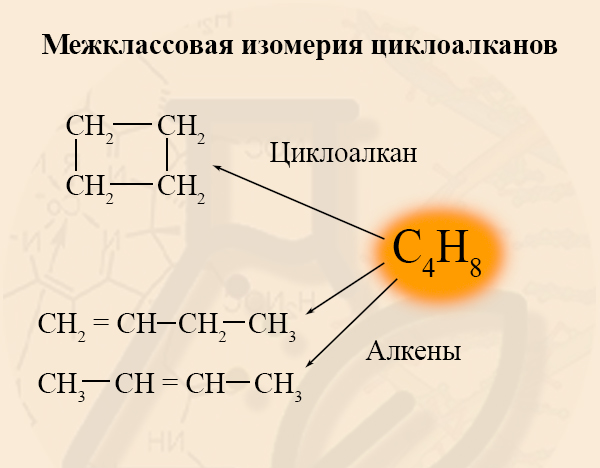
- Межклассовая изомерия: циклоалканы изомерны алкенам.
Формуле С3Н6 соответствуют циклопропан и пропен.
Геометрическая (цис-транс-) изомерия
У циклоалканов с двумя заместителями, расположенными у соседних атомов углерода в цикле цис-транс-изомерия обусловлена различным взаимным расположением в пространстве заместителей относительно плоскости цикла.
В цис-изомерах заместители находятся по одну сторону от плоскости цикла, в транс-изомерах – заместители расположены по разные стороны.
В молекуле 1,2-диметилциклопропана две группы СН3 могут находиться по одну сторону от плоскости цикла (цис-изомер) или по разные стороны (транс-изомер):
Для 1,1-диметилциклопропана цис-транс-изомерия не характерна.
Номенклатура циклоалканов
В названиях циклоалканов используется префикс -ЦИКЛО.
Название циклоалканов строится по следующим правилам:
1. Цикл принимают за главную углеродную цепь. При этом считают, что углеводородные радикалы, которые не входят в главной цепь, являются в ней заместителями.
2. Нумеруют атомы углерода в цикле так, чтобы атомы углерода, которые соединены с заместителями, получили минимальные возможные номера. Причем нумерацию следует начинать с более близкого к старшей группе конца цепи.
3. Называют все радикалы, указывая впереди цифры, которые обозначают их расположение в главной цепи.
Для одинаковых заместителей эти цифры указывают через запятую, при этом количество одинаковых заместителей обозначается приставками ди- (два), три- (три), тетра- (четыре), пента- (пять) и т.д.
Например, 1,1-диметилциклопропан или 1,1,3-триметилциклопентан.
4. Названия заместителей со всеми приставками и цифрами располагают в алфавитном порядке.
Например: 1,1-диметил-3-этилциклопентан.
5. Называют углеродный цикл.
Химические свойства циклоалканов
Циклоалканы с малым циклом (циклопропан, циклобутан и их замещенные гомологи) из-за большой напряженности в кольце могут вступать в реакции присоединения.
1. Реакции присоединения к циклоалканам
Чем меньше цикл и чем больше угловое напряжение в цикле, тем легче протекают реакции присоединения. Способность вступать в реакции присоединения уменьшается в ряду: циклопропан > циклобутан > циклопентан.
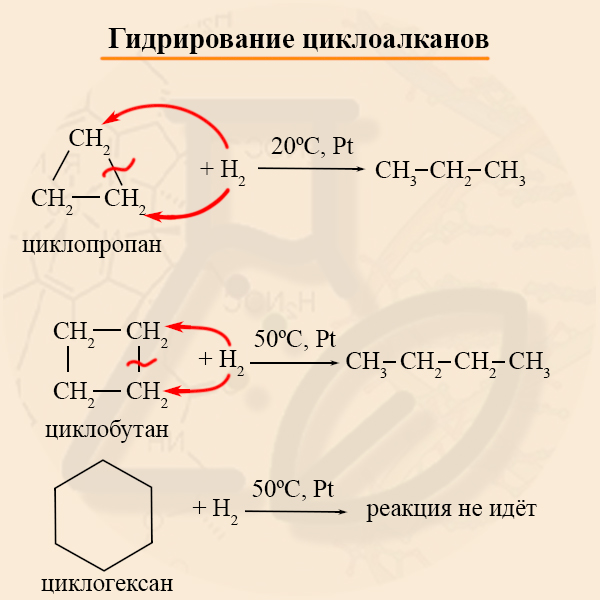
1.1. Гидрирование циклоалканов
С водородом могут реагировать малые циклы, а также (в жестких условиях) циклопентан. При этом происходит разрыв кольца и образование алкана.
Циклопропан и циклобутан довольно легко присоединяют водород при нагревании в присутствии катализатора:
Циклопентан присоединяет водород в жестких условиях:
Бромирование протекает более медленно и избирательно.
Циклогексан и циклоалканы с большим число атомов углерода в цикле с водородом не реагируют.
1.2. Галогенирование циклоалканов
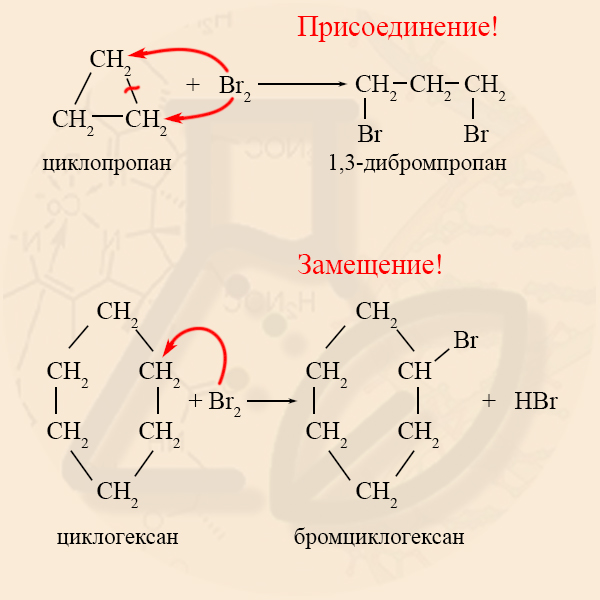
Циклопропан и циклобутан реагируют с галогенами, при этом тоже происходит присоединение галогенов к молекуле, сопровождающееся разрывом кольца.
Например. Циклопропан присоединяет бром с образованием 1,3-дибромпропана:
1.3. Гидрогалогенирование
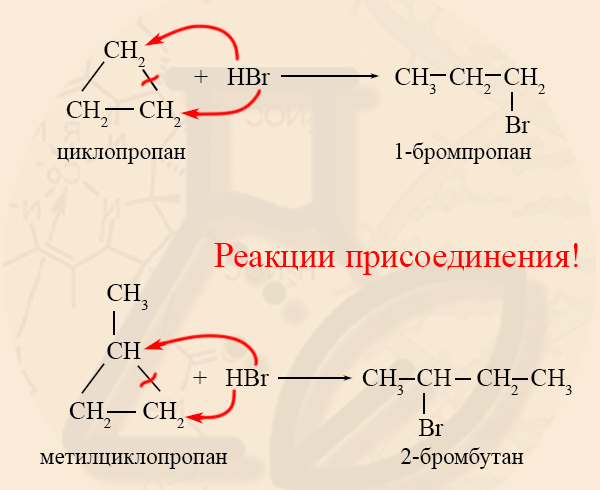
Циклопропан и его гомологи с алкильными заместителями у трехчленного цикла вступают с галогеноводородами в реакции присоединения с разрывом цикла.
Например, циклопропан присоединяет йодоводород.
Присоединение галогеноводородов к гомологам циклопропана с заместителями у трехатомного цикла (метилциклопропан и др.) происходит по правилу Марковникова.
Например, при присоединении бромоводорода к метилциклопропану преимущественно образуется 2-бромбутан
2. Реакции замещения
Поэтому большие циклы гораздо более устойчивы, чем малые, и реакции присоединения с разрывом связей С-С для них не характерны. В химических реакциях они ведут себя подобно алканам, вступая в реакции замещения без разрыва кольца.
2.1. Галогенирование
Галогенирование циклопентана, циклогексана и циклоалканов с большим количеством атомов углерода в цикле протекает по механизму радикального замещения.
Например, при хлорировании циклопентана на свету или при нагревании образуется хлорциклопентан
При хлорировании метилциклопентана замещение преимущественно протекает у третичного атома углерода:
2.2. Нитрование циклоалканов
При взаимодействии циклоалканов с разбавленной азотной кислотой при нагревании образуются нитроциклоалканы.
Например, нитрование циклопентана.
2.3. Дегидрирование
При нагревании циклоалканов в присутствии катализаторов протекает дегидрирование – отщепление водорода.
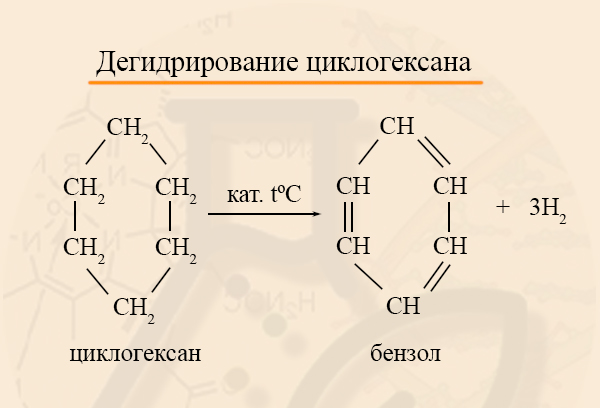
Циклогексан и его производные дегидрируются при нагревании и под действием катализатора до бензола и его производных.
Например, бензол образуется при дегидрировании циклогексана.
Например, при отщеплении водорода от метилциклогексана образуется толуол.
3. Окисление циклоалканов
3.1. Горение
Как и все углеводороды, алканы горят до углекислого газа и воды. Уравнение сгорания циклоалканов в общем виде:
CnH2n + 3n/2O2 → nCO2 + nH2O + Q
Например, горение циклопентана.
2C5H10 + 15O2 → 10CO2 + 10H2O + Q
3.2. Окисление
При окислении циклогексана азотной кислотой или в присутствии катализатора образуется адипиновая (гександиовая) кислота:
Получение циклоалканов
1. Дегидрирование алканов
Алканы с длинным углеродным скелетом, содержащие 5 и более атомов углерода в главной цепи, при нагревании в присутствии металлических катализаторов образуют циклические соединения.
При этом протекает дегидроциклизация – процесс отщепления водорода с образованием замкнутого цикла.
Пентан и его гомологи, содержащие пять атомов углерода в главной цепи, при нагревании над платиновым катализатором образуют циклопентан и его гомологи:
Алканы с углеродной цепью, содержащей 6 и более атомов углерода в главной цепи, при дегидрировании образуют устойчивые шестиатомные циклы, т. е. циклогексан и его гомологи, которые далее превращаются в ароматические углеводороды.
Гексан при нагревании в присутствии оксида хрома (III) в зависимости от условий может образовать циклогексан и потом бензол:
Гептан при дегидрировании в присутствии катализатора образует метилциклогексан и далее толуол:
Дегидроциклизация алканов — важный промышленный способ получения циклоалканов.
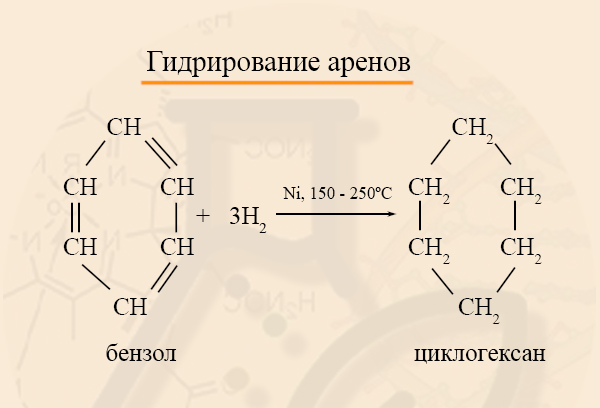
2. Гидрирование бензола и его гомологов
При гидрировании бензола при нагревании и в присутствии катализатора образуется циклогексан:
При гидрировании толуола образуется метилциклогексан:
Этим способом можно получить только циклогексан и его гомологи с шестичленным кольцом.
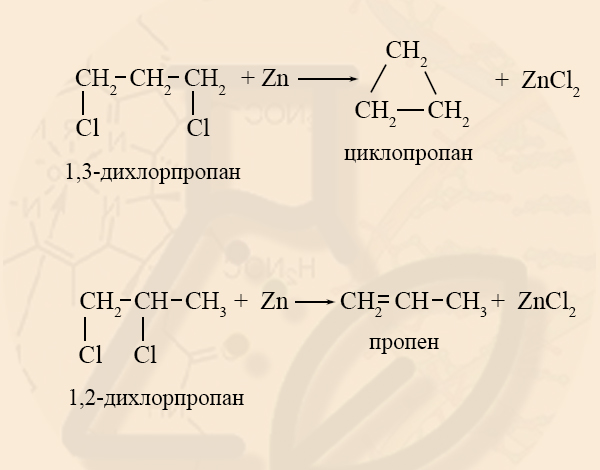
3. Дегалогенирование дигалогеналканов
При действии активных металлов на дигалогеналканы, в которых между атомами галогенов находится три и более атомов углерода.
Например, 1,4-дибромбутан реагирует с цинком с образованием циклобутана
Таким образом можно синтезировать циклоалканы заданного строения, в том числе циклоалканы с малыми циклами (С3 и С4).
План урока:
Формула и строение циклоалканов
Номенклатура и изомерия циклоалканов
Методы получения циклоалканов
Физические свойства циклоалканов
Химические свойства циклоалканов
Области применения циклоалканов
Формула и строение циклоалканов
Углеродным атомам характерна sp3-гибридизация и формирование четырех сигма-связей (σ-связи) С-Н и С-С. От размеров цикла зависят свойства вещества. У первых двух представителей гомологического ряда валентный угол равен не 109˚35’, как в алканах, а меньше. Из-за возникающего напряжения в молекуле эти циклы имеют высокую реакционную способность.
«Банановые» σ-связи в циклопропане – особенность строения циклоалканов. Они расположены так, что соединяют ядра атомов углерода не прямой, а дугообразной линией. «Банановые» связи схожи с π-связями, т.к. легко рвутся. Они необходимы для уменьшения напряжения внутри цикла.
Рис. Малые циклопропаны. А, б, в – «банановые» связи циклоалканов; г – конформации циклоалканов. Источник
Другие нафтены имеют особенность – пространственное строение. В циклобутане есть перегиб между первым и третьим углеродным атомами. Циклопентан представлена в конформации «конверт», а циклогексан – в «кресло» и «ванна».
Общая формула циклоалканов: CnH2n, где n≥3.
Номенклатура и изомерия циклоалканов
Название состоит из приставки «цикло» и названия алкана с определенным количеством углеродных атомов. Циклоалканы подразделяются на малые и большие циклы. К первой группе относятся циклопропан и циклобутан, а ко второй все остальные вещества. Соединения этого класса часто изображают в виде геометрических фигур, где количество углов соответствует числу атомов углерода.
Для циклоалканов свойственно два вида изомерии – структурная и пространственная. Структурная включает в себя:
- изомерию углеродного скелета (расположение атомов может меняться как в цикле, так и в боковой цепи),
- изомерию положения заместителей в кольце,
- межклассовую изомерию (изомерны алкенам).
Пространственная включает в себя:
- цис-транс-изомерию,
- зеркальную изомерию (основана на существовании нескольких оптических изомеров),
- поворотную изомерию (основана на повороте относительно σ-связи).
Источник
Методы получения циклоалканов
В промышленном производстве циклоалканы получают двумя способами.
- Гидрирование аренов при нагревании с катализатором Ni
- Дегидрирование алканов при нагревании с катализатором
Циклы, имеющие шесть и более углеродных атома, получают под воздействием оксида хрома (III).
В лабораториях циклоалканы получают с помощью дегалогенирования дигалогеналканов. Особенность этого метода заключается в том, что галогены должны находиться на концах молекулы алкана.
Физические свойства циклоалканов
Циклоалканы во многом схожи с алканами. Первые два представителя гомологичного ряда – газы, следующие два – жидкости (они входят во фракции нефти), последующие соединения циклоалканов – твердые вещества. Температуры плавления и кипения выше, чем алканов с соответствующим количеством углеродных атомов. Это объясняется плотным расположением атомов внутри молекулы. Циклоалканы не растворимы в воде, но растворимы в органических растворителях.
Химические свойства циклоалканов
Свойства циклоалканов различны и меняются по мере изменения размеров молекулы. Малым циклам характерны реакции присоединения, а большим – замещения.
Реакции присоединения
Малые циклы хотя и проявляют насыщенность, но им не характерны свойства предельных углеводородов. Это связано с тем, что у первых двух простейших представителей циклоалканов валентные углы меньше. Для них свойственно напряжение внутри кольца и тяга к раскрытию при воздействии реагентов.
- Гидрирование при воздействии катализатора и высоких температур
- Галогенирование
- Гидрогалогенирование при нагревании
Реакции гидрогалогенирования гомологов циклоалканов осуществляется по правилу Марковникова.
Реакции замещения
Циклы с шестью и более углеродными атомами наиболее устойчивы из-за отсутствия углового напряжения.
- Галогенирование под действием света
У гомологов циклоалканов галоген замещается у третичного атома углерода.
Окисление
Уравнения реакции окисления характерны как для малых, так и для больших циклов.
Области применения циклоалканов
Нафтены нашли широкое применение в качестве:
- анестезирующих ингаляторов;
- продукта народного хозяйства;
- растворителей и др.
Также их применяют в получении полупродуктов при производстве синтетических волокон, адипиновой кислоты, циклогексанола. Применение циклоалканов актуально для получения аренов в нефтяной промышленности.
Циклоалканы
Материал по химии
- Основные характеристики циклоалканов:
- Номенклатура циклоалканов
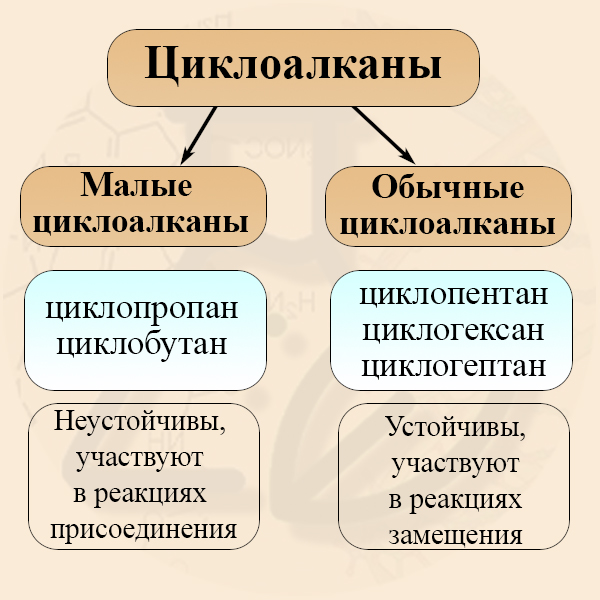
- Малые и обычные циклоалканы
- Строение молекул циклоалканов
- Изомерия циклоалканов
- Химические свойства циклоалканов
- Таблица — Сравнение химических свойств циклоалканов с другими углеводородами
- Получение циклоалканов
- Физические свойства циклоалканов
Циклоалканы – это углеводороды, в которых атомы углерода образуют кольца (иными словами, циклы) и не имеют кратных связей. Циклоалканы в разных учебниках могут называться по-разному: алициклическими соединениями, алифатическими циклами, циклопарафинами, нафтенами (так как содержатся в нефти).
Если Вы уже знакомы с данной темой, попробуйте решить задание:
Задание в формате ЕГЭ с ответом:
Выберите три верных утверждения о свойствах и строении циклоалканов.
- В циклоалканах на одну свесь С-С больше, чем в алканах с таким же количеством углерода
- Цис- и трансизомеры легко превращаются друг в друга
- Малые циклоалканы менее устойчивы, чем нормальные
- Межклассовыми изомерами циклоалканов являются циклоалкены
- Для циклоалканов характерна sp3-гибридизация
- Циклопентан относят к малым циклам
Вернитесь к заданию после прочтения материала, если Вы пока не понимаете, о чём речь.
Основные характеристики циклоалканов:
- Предельные (не имеют кратных связей)
- Атомы находятся в sp3-гибридицазии
- Только σ-связи (однако есть так называемые «банановые», грубо говоря, это деформированные σ-связи)
- Общая формула циклоалканов CnH2n
Номенклатура циклоалканов
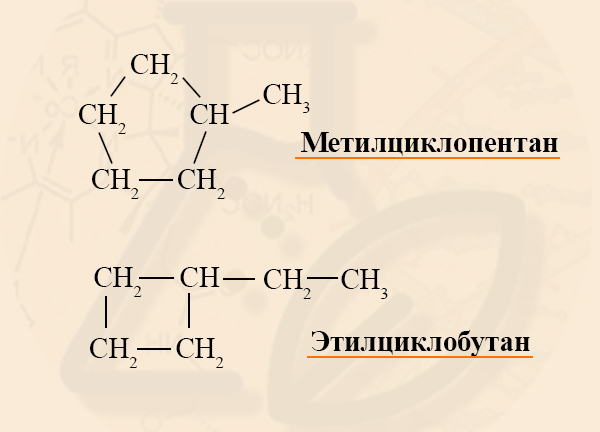
Называются циклоалканы подобно алканам, только с приставкой «цикло». Если трехуглеродный алкан называют пропаном, то трехуглеродный цикл – циклопропаном.
Если в кольце есть один заместитель, то его называют, не указывая номер углерода, так как в этом нет смысла. Номенклатура радикалов такая же, как в алканах, название основного вещества и радикала пишут слитно:
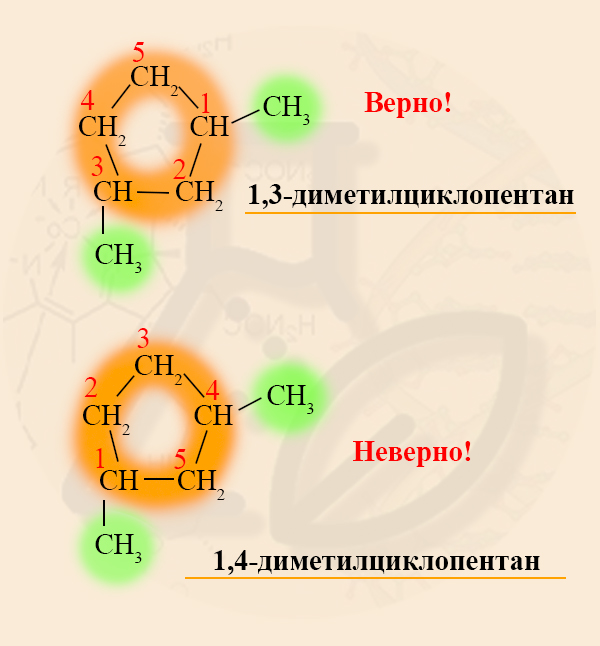
Если в кольце два или более заместителя, то при составлении названия пользуются следующими правилами:
- Нумерацию углеродов кольца производят таким образом, чтобы заместители получили наименьшие номера.
- Одинаковые радикалы называют с приставкой «ди-», «три-» и так далее, как это было в номенклатуре алканов.
- Заканчивают номенклатуру названием цикла:
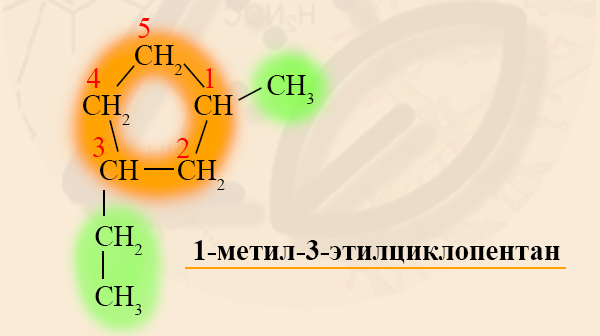
Разноименные радикалы называют в порядке алфавита, то есть, если в кольце есть заместитель CH3 – Метил и CH3-CH2 – Этил, то первый номер обязательно займет метил, так как буква «М» стоит в алфавите раньше, чем «Э».
Малые и обычные циклоалканы
По размеру кольца циклоалканы принято разделять на малые и нормальные циклы (также встречается деление циклоалканов на малые, средние и большие, но такой способ их классификации встречается реже). К малым циклоалканам относят циклопропан и циклобутан, к обычным или средним циклам относят циклопентан, циклогексан и циклогептан. Малые и обычные циклы значительно отличаются друг от друга по ряду химических свойств:
Чтобы понять, в чем причина таких значительных отличий внутри одной гомологической группы, следует разобрать строение циклоалканов.
Строение молекул циклоалканов
- Строение молекулы циклопропана
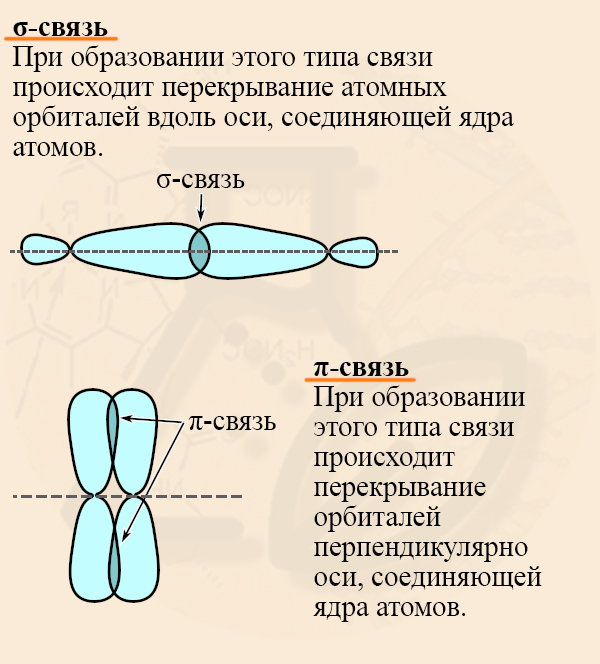
Для начала следует вспомнить особенности σ- (сигма) и π-связей (пи-связей). Для веществ с простыми (ПРЕДЕЛЬНЫМИ) связями характерна sp3-гибридизация (то есть все четыре орбитали – 1s и 3p гибридизуются, усредняются), а между атомами углерода образуются σ- связи. При образовании этого типа связи происходит перекрывание атомных орбиталей вдоль оси, соединяющей ядра атомов.
У непредельных (имеющих двойные или тройные связи) веществ гибридизованы не все орбитали, и между негибридизованными может образовываться π-связь. При образовании этого типа связи происходит перекрывание орбиталей перпендикулярно оси, соединяющей ядра атомов.
К чему же мы упоминаем π-связь, когда в циклоалканах нет непредельных связей?
Для sp3-гибридизации характерен угол связи равный 109,5º, но как расположить три углерода в цикле, чтобы такой угол сохранился (Вы ведь помните, что у равностороннего треугольника углы равны 60º)? К сожалению, никак! Чтобы трехуглеродная молекула образовала кольцо (треугольник), углы связей придется сжать, при этом возникает угловая напряженность связи.
Скажем простыми словами: 4 электрона (ведь столько неспаренных электронов содержится у атома углерода в возбужденном состоянии, что и определяет валентность IV атома углерода в органических соединениях) способны «терпеть» друг друга, если их орбитали расположены максимально удаленно друг от друга. Такое удаление обеспечивается расположением четырех гибридных орбиталей в форме тетраэдра, угол между орбиталями в нем составляет 109,5º. Такое мы наблюдаем в алканах.
Вернемся же к малым циклоалканам. Чтобы замкнулось кольцо, две из четырех орбиталей должны находиться под меньшим углом друг к другу, из-за чего стремятся «разжаться» и прийти снова в более комфортное состояние тетраэдра, поэтому малые циклы участвуют в реакциях присоединения, при которых цикл разрывается и орбитали углеродов встают в свое наиболее устойчивое положение.
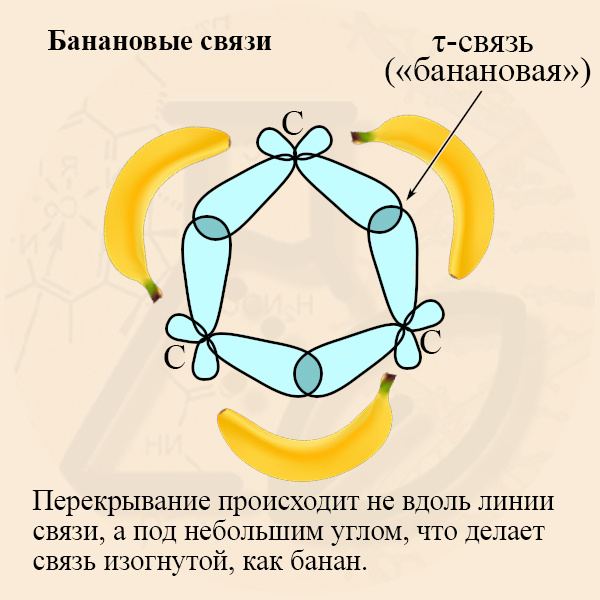
Хотелось бы добавить, что гибридизованные орбитали углеродов в малых циклах перекрываются не как обычно – по линии, когда образуется σ-связь, перекрытие получается полубоковым. Такая связь получила название τ-связи или «банановой» связи (на рисунке изображены только С – С связи, участвующие в образовании кольца):
Обобщим:
- σ – связь является прочной, если молекула имеет только такой тип связей, то для нее характерны реакции замещения.
- π – менее прочная, наличие такой связи в молекуле обеспечивает возможность осуществления реакций присоединения.
- τ-связь (тау-связь) – является промежуточной, она менее прочна, чем σ-связь, поэтому для малых циклов характерны реакции присоединения.
- Строение циклобутана
Чем больше углов в фигуре, тем больше может быть угол связи, кроме того, четырехуглеродное кольцо может быть не плоским, что также позволяет снять «напряженность» связей. Для циклобутана тоже характерны реакции присоединения, но идут они гораздо труднее, чем у циклопропана (то есть циклобутан устойчивее своего трехуглеродного гомолога).
За счет неплоской структуры циклопентану и циклогексану удается избежать углового напряжения, поэтому они более стабильны:
Изомерия циклоалканов
- Структурная изомерия циклоалканов
Этот тип изомерии связан положением заместителей или размером цикла. Помните, что изомерами называют вещества с одинаковым составом (одинаковой брутто-формулой), но разным строением:
- Межклассовая изомерия циклоалканов
Межклассовыми изомерами циклоалканов являются алкены. У этих двух групп одинаковая общая формула CnH2n. Так как общая формула у этих двух классов равна, Вы смело можете говорить, что циклоалкан и алкен являются изомерами, если они содержат одинаковое количество углерода.
- Пространственная геометрическая изомерия (цис-транс-изомерия)
Цис- и трансизомерия – это возможность существования двух, казалось бы, совершенно одинаковых веществ в двух формах, отличающихся по некоторым физическим или даже химическим свойствам. Рассмотрим, к примеру, цис-1,2-диметилциклопропан и транс-1,2-диметилциклопропан. Если одинаковые заместители находятся либо только сверху плоскости связи, либо только снизу, то такой изомер называют «цис-…», если одинаковые заместители находятся по разные стороны от плоскости связи, то такой изомер называют «транс-…».
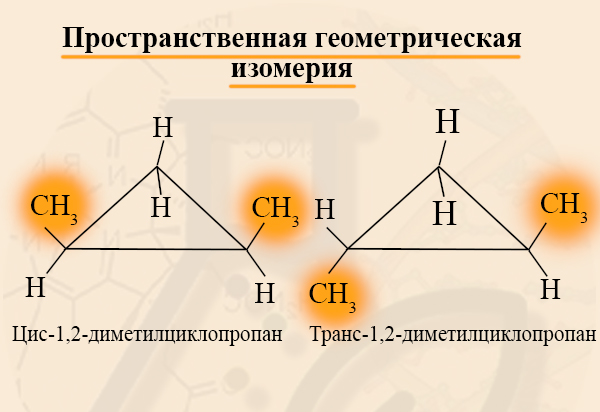
Для каких циклоалканов характерна цис-трансизомерия? Для тех, которые содержат два заместителя на РАЗНЫХ атомах углерода кольца. При этом, стоит отметить, что цис- и трансизомеры не могут переходить друг в друга, их стоит рассматривать, как две совершенно разные молекулы.
Пример задания из КИМ ЕГЭ:
Выберите все вещества, являющиеся изомерами циклопентана:
1) циклобутан; 2) метилциклобутан; 3) этилциклопропан; 4) метилциклопропан; 5) 2-метилбутен-2.
Запишите в графу ответов последовательность цифр в порядке возрастания.
Химические свойства циклоалканов
Химические свойства малых и средних (обычных) циклов в значительной степени отличаются. О причинах этого написано выше.
- Гидрирование циклоалканов
В реакцию с водородом вступают преимущественно малые циклы, реакцию проводят на никелевом или платиновом катализаторе. На примере гидрирования хорошо заметно увеличение устойчивости циклов с ростом кольца.
- Галогенирование циклоалканов
Реакции галогенирования характерны как для малых циклов, так и для нормальных, но в механизме реакций есть существенные отличия: малые циклы вступают с галогенами в реакции ПРИСОЕДИНЕНИЯ, а нормальные – в реакции ЗАМЕЩЕНИЯ.
- Гидрогалогенирование циклоалканов
Гидрогалогенирование возможно только для малых циклов, причем, если циклоалкан содержит заместитель, то реакция идет по правилу Марковникова.
- Дегидрирование циклоалканов
При дегидрировании циклогексана и других его гомологов с шестью атомами углерода в кольце, образуются арены.
Задание по образцу ФИПИ:
Выберите все вещества, с которыми может реагировать циклопентан:
1) водород; 2) кислород; 3) азот; 4) хлор на свету; 5) бромоводород.
Запишите в графу ответов последовательность цифр в порядке возрастания.
Таблица — Сравнение химических свойств циклоалканов с другими углеводородами
Интересно рассмотреть циклоалканы в сравнении с алканами и алкенами
|
Реагент |
Алкан |
Малый цикл |
Нормальный цикл |
Алкен |
|
Водород |
Реакция не идет |
Присоединение с образованием алкана |
Реакция не идет |
Присоединение с образованием алкана |
|
Хлор/бром |
Реакция замещения, образуется моногалогеналкан |
Реакция присоединения, образуется дигалогеналкан |
Реакция замещения с сохранением цикла |
Реакция присоединения с образованием дигалогеналкана |
|
Хлороводород/ бромоводород |
Реакция не идет |
Реакция присоединения |
Реакция не идет |
Реакция присоединения |
Из таблицы видно, что малые циклы больше похожи на алкены, а нормальные циклы – на алканы.
Попробуйте решить задание ЕГЭ:
Выберите три верных ответа из шести. Для циклогексана, в отличие от циклопропана, характерно:
- С галогенами вступает в реакции замещения
- Реагирует с водой
- Атомы углерода, принадлежащие циклу, не образуют плоскую фигуру
- Окисляется при горении на воздухе
- Не реагирует с бромоводородом
- Реагирует с метаном
Получение циклоалканов
- Получение циклоалканов из аренов
Из бензола и его гомологов можно получить циклогексан и его гомологи:
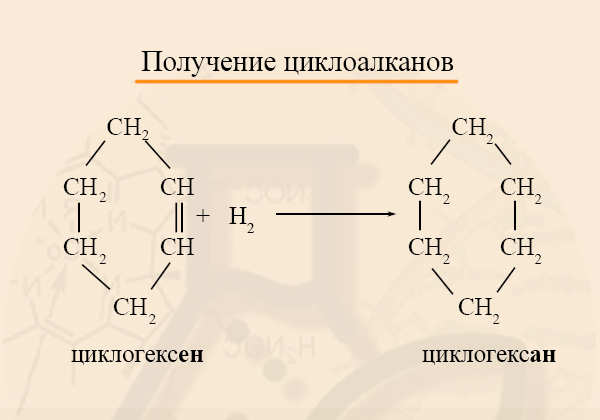
- Получение циклоалканов из циклоалкенов
Аналогично предыдущему методу получения, исходное вещество гидрируется:
- Получение циклоалканов из дигалогеналканов
Условием образования циклоалкана из дигалогеналкана является то, что галогены должны находиться хотя бы через 1 атом углерода. Если вещество имеет заместитель на соседних атомах углерода, то образуется не циклоалкан, а алкен:
Выберите все вещества, из которых можно получить циклобутан напрямую (одной реакцией):
1) бутен-2; 2) 1,2-дибромбутан; 3) циклобутен; 4) 1,4-дихлорбутан; 5) хлорэтан.
Запишите в графу ответов последовательность цифр в порядке возрастания.
Физические свойства циклоалканов
- Физические свойства циклоалканов близки к таковым у соответствующих алканов, несколько отличаются температура кипения и плотность (у циклоалканов она выше).
- Циклоалканы нерастворимы в воде (циклоалканы неполярные, а вода – полярный растворитель).
- Но циклоалканы растворимы в эфирах и четыреххлористом углероде (это неполярные растворители, неполярное хорошо растворяется в неполярном).
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Циклоалканы (циклопарафины, нафтены) — циклические насыщенные углеводороды, по химическому строению близкие к алканам. Содержат только
простые одинарные сигма связи (σ-связи), не содержат ароматических связей.
Циклоалканы имеют большую плотность и более высокие температуры плавления, кипения, чем соответствующие алканы. Общая формула их
гомологического ряда — CnH2n.
Номенклатура и изомерия циклоалканов
Названия циклоалканов формируются путем добавления приставки «цикло-» к названию алкана с соответствующим числом:
циклопропан, циклобутан и т.д.
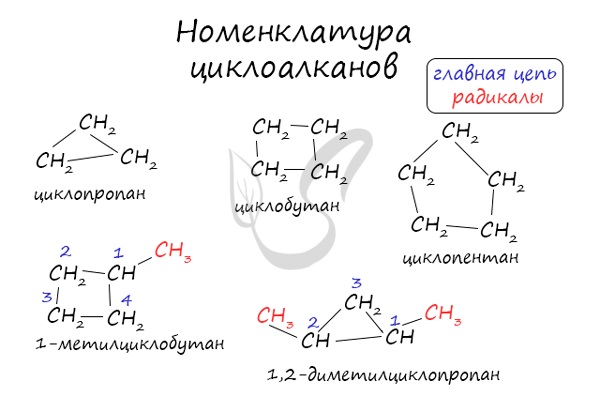
Как и у алканов, атомы углерода циклоалканов находятся в sp3 гибридизации.
Помимо изомерии углеродного скелета, для циклоалканов характерна межклассовая изомерия с алкенами и пространственная геометрическая изомерия в виде
существования цис- и транс-изомеров.
Получение циклоалканов
В промышленности циклоалканы получают несколькими способами:
- Из ароматических углеводородов
- Циклизация алканов
Циклоалканы можно получить гидрированием (присоединением водорода) бензола и его гомологов.

При наличии катализатора и повышенной температуры алканы способны образовывать цикл, отщепляя при этом водород.
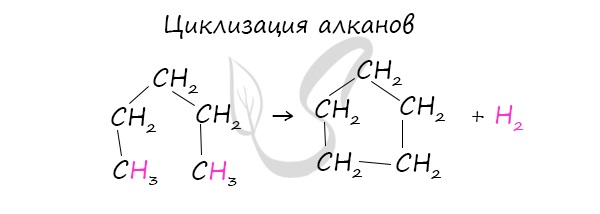
В лабораторных условиях циклоалканы можно получить реакцией дегалогенирования дигалогеналканов.
- Дегалогенирование дигалогеналканов (внутримолекулярная реакция Вюрца)

Химические свойства циклоалканов
Важно заметить, что циклопропан и циклобутан вступают в реакции присоединения, проявляя свойства ненасыщенных соединений. Для циклопентана и циклогексана
реакции присоединения не характерны, они преимущественно вступают в реакции замещения.
- Гидрирование
- Галогенирование
- Гидрогалогенирование
- Дегидрирование
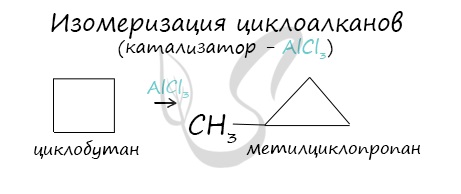
- Изомеризация
Наиболее легко в реакции гидрирования вступают циклопропан и циклобутан. Циклопентан и циклогексан не вступают в реакции гидрирования (в рамках вопросов ЕГЭ — не вступают, но на самом деле эти реакции идут, просто крайне затруднены).

Без освещения реакция циклопропана и циклобутана с хлором идет по типу присоединения. При освещении хлор образует свободные радикалы, реакция
идет, как и у алканов, по механизму замещения.
У циклопентана и циклогексана реакция идет только путем замещения.
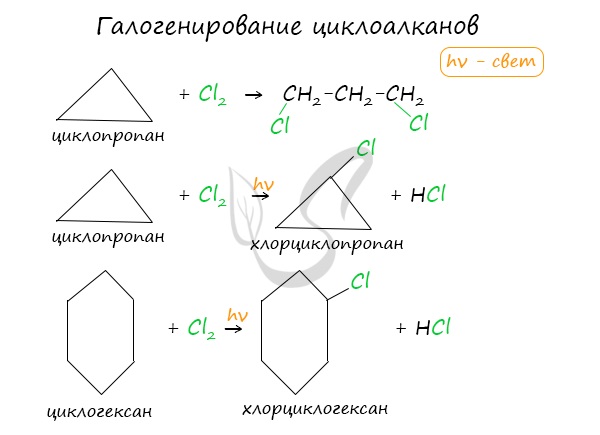
В реакции гидрогалогенирования, протекающие по типу присоединения, вступают циклопропан и циклобутан.
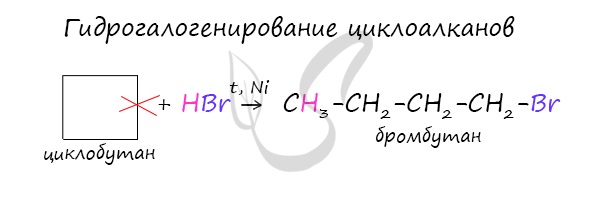
При отщеплении водорода от циклогексана образуется бензол, при наличии радикалов — гомологи бензола.

В ходе нагревания с катализатором — AlCl3 циклоалканы образуют изомеры.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.