Физические свойства
Нитрат натрия NaNO3 — соль щелочного металла натрия и азотной кислоты. Белое вещество, весьма гигроскопичное, которое плавится без разложения, при дальнейшем нагревании разлагается.
Относительная молекулярная масса Mr = 84,99; относительная плотность для тв. и ж. состояния d = 2,266; tпл = 306,5º C;
Способ получения
1. Нитрат натрия можно получить путем взаимодействия гидроксида натрия и разбавленной азотной кислоты, образуется нитрат натрия и вода:
NaOH + HNO3 = NaNO3 + H2O
2. В результате взаимодействия горячего гидроксида натрия, оксида азота (IV) и кислорода образуется нитрат натрия и вода:
4NaOH + 4NO2 + O2 = 4NaNO3 + 2H2O
3. В результате реакции между горячим гидроксидом натрия, оксидом натрия (IV) и кислородом, происходит образование нитрата натрия и воды:
4NO2 + O2 + 4NaOH = 4NaNO3 + 2H2O
4. При комнатной температуре, в результате взаимодействия оксида азота (IV) и натрия образуется нитрат натрия и газ оксид азота (II):
2NO2 + Na = NO↑ + NaNO3
5. При смешивании горячего пероксида водорода и нитрита азота происходит образование нитрата натрия и воды:
NaNO2 + H2O2 = NaNO3 + H2O
Качественная реакция
Качественная реакция на нитрат натрия — взаимодействие с медью при нагревании в присутствии концентрированной кислоты:
1. При взаимодействии с серной кислотой и медью, нитрат натрия образует сульфат натрия, нитрат меди, газ оксид азота и воду:
NaNO3 + H2SO4 + Cu = Na2SO4 + Cu(NO3)2 + NO2↑ + H2O
Химические свойства
1. Hитрат натрия разлагается при температуре 380–500º С с образованием нитрита натрия и кислорода:
2NaNO3 = 2NaNO2 + O2
2. Нитрат натрия может реагировать с простыми веществами:
2.1. Нитрат натрия реагирует со свинцом при температуре выше 350 ºС. При этом образуется нитрит натрия и оксид свинца:
NaNO3 + Pb = NaNO2 + PbO
2.2. Нитрат натрия реагирует при комнатной температуре с цинком и разбавленной хлороводородной кислотой с образованием нитрита натрия и воды:
NaNO3 + Zn + 2HCl = NaNO2 + ZnCl2 + H2O,
NaCl – хлорид натрия;
NaNO3 – нитрат натрия;
CaCl2 – хлорид кальция;
KHSO4 – гидросульфат калия;
Al(NO3)3 – нитрат алюминия;
K3PO4 – ортофосфат калия;
Na2SO4 – сульфат натрия;
Na2S – сульфид натрия;
Na2SO3 – сульфит натрия;
Ca(HS)2 – гидросульфид кальция;
FeSO4 – сульфат железа (II);
AgNO3 – нитрат серебра;
Fe(SO4)3 – сульфат железа (III);
Na2CO3 – карбонат натрия;
Cr2(SO4)3 – сульфат хрома (III);
NaHCO3 – гидрокарбонат натрия;
Ca(HCO3)2 – гидрокарбонат кальция.
Хлориды — NaCl, CaCl2;
Сульфаты — Na2SO4, FeSO4, Fe(SO4)3, Cr2(SO4)3;
Нитраты — NaNO3, Al(NO3)3, AgNO3;
Гидрокарбонаты — NaHCO3, Ca(HCO3)2;
Гидросульфаты — KHSO4;
Фосфаты — K3PO4;
Сульфиды – Na2S.
|
Составьте формулы солей натрия, кальция и алюминия азотной, серной и фосфорной кислот. Какие из этих солей растворимы в воде? (Габриелян. Химия. 8 класс. Параграф 17, № 2) 1) Натрий Na.
2) Кальций Ca.
3) Алюминий Al.
автор вопроса выбрал этот ответ лучшим Arderik 4 месяца назад NaNO3- растворима Ca(NO3)2-растворима Al(NO3)3-растворима Na2SO4-растворима CaSO4-малорастворима Al2(SO4)3-растворима Na3PO4-растворима Ca3(PO4)2-растворима AlPO4-нерастворима Знаете ответ? |
Смотрите также: ВПР по химии 8 класс 2020, задания, ответы, демоверсии, где найти? Химия 8 класс учебник Аббасов, где читать онлайн, краткое содержание? Химия 8 класс учебник Усманова, Сакарьянова, где читать онлайн? Химия 8 класс учебник Григорович, где читать онлайн, краткое содержание? Химия 8 класс учебник Еремин, Кузьменко, Дроздов, Лунин, где читать онлайн? Химия 8 класс учебник Габриелян, где читать онлайн, краткое содержание? Химия 8 класс учебник Кузнецова, Титова, Гара, где читать онлайн? ВПР 2022, химия, 8 класс, все варианты с ответами — где найти, скачать? ВПР по химии 8 класс 2021, задания, ответы, демоверсии, где найти? ВПР по химии 8 класс с ответами 2019 год все варианты — где найти/скачать? |
Формула нитрата натрия
Определение и формула нитрата натрия
Плавится без разложения, но разлагается при дальнейшем нагревании. Хорошо растворяется в воде (не гидролизуется). Кристаллогидратов не образует. Практически не растворяется в концентрированной азотной кислоте. Сильный окислитель при спекании.
Рис. 1. Нитрат натрия. Внешний вид.
Химическая формула нитрата натрия
Химическая формула нитрата натрия NaNO3. Химическая формула показывает качественные и количественный состав молекулы (сколько и каких атомов присутствует в ней). По химической формуле можно вычислить молекулярную массу вещества (Ar(Na) =23а.е.м., Ar(N) = 14 а.е.м., Ar(O) = 16 а.е.м.):
Mr(NaNO3) = Ar(Na) + Ar(N) + 3×Ar(O);
Mr(NaNO3) = 23 + 14 + 3×16 = 23 + 14 + 48 = 85.
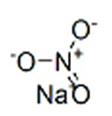
Структурная (графическая) формула нитрата натрия
Структурная (графическая) формула вещества является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы. Ниже представлена графическая формула нитрата натрия:
Ионная формула
Нитрат натрия электролит, поэтому он способен диссоциировать в водном растворе на ионы согласно следующему уравнению:
NaNO3 ↔ Na+ + NO3—.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |
Составьте формулы солей натрия, кальция и алюминия для следующих кислот: азотной, серной и фосфорной. Дайте их названия. Какие из солей растворимы в воде? Вот такое у меня задание, но мне сейчас очень важно чтобы мне объяснили одну вещь. Сейчас приведу пример. Например, формула натрия азота NaNO3, а вот формула кальция азота почему-то Ca(NO3)2. Тоесть почему-то цифру 2 в конце приписали, ну тоесть индекс. Я надеюсь, что хотя-бы кто-нибудь меня понял. Тоесть мне надо объяснить, почему в конце кальция азота поставили индекс 2, а в натрии азота ее нет. И также целый номер пожалуйста объясните, если опять где-то в конце попадется такая же проблема. И также почему в натрии серы Na2SO4 посередине между натрием и серой стоит индекс 2, а в кальции серы CaSO4 посередине нету индекса 2. Как это работает? Также если еще во всем задании попадутся такие же посередине проблемы, назову их так, то тоже объясните. Пожалуйста!


