Большинство органических соединений имеют молекулярное строение. Атомы в веществах с молекулярным типом строения всегда образуют только ковалентные связи друг с другом, что наблюдается и в случае органических соединений. Напомним, что ковалентным называется такой вид связи между атомами, который реализуется за счет того, что атомы обобществляют часть своих внешних электронов с целью приобретения электронной конфигурации благородного газа.
По количеству обобществлённых электронных пар ковалентные связи в органических веществах можно разделить на одинарные, двойные и тройные. Обозначаются данные типы связей в графической формуле соответственно одной, двумя или тремя чертами:
Кратность связи приводит к уменьшении ее длины, так одинарная С-С связь имеет длину 0,154 нм, двойная С=С связь – 0,134 нм, тройная С≡С связь – 0,120 нм.
Типы связей по способу перекрывания орбиталей
Как известно, орбитали могут иметь различную форму, так, например, s-орбитали имеют сферическую, а p-гантелеобразную форму. По этой причине связи также могут отличаться по способу перекрывания электронных орбиталей:
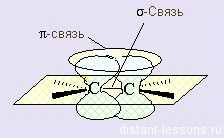
• ϭ-связи – образуются при перекрывании орбиталей таким образом, что область их перекрывания пересекается линией, соединяющей ядра. Примеры ϭ-связей:
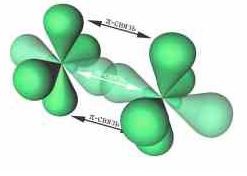
• π-связи – образуются при перекрывании орбиталей, в двух областях – над и под линией соединяющей ядра атомов. Примеры π-связей:
Как узнать, когда в молекуле есть π- и ϭ-связи?
При ковалентном типе связи ϭ-связь между любыми двумя атомами есть всегда, а π-связь имеет только в случае кратных (двойных, тройных) связей. При этом:
- Одинарная связь – всегда является ϭ-связью
- Двойная связь всегда состоит из одной ϭ- и одной π-связи
- Тройная связь всегда образована одной ϭ- и двумя π-связями.
Укажем данные типы связей в молекуле бутин-3-овой кислоты:
Гибридизация орбиталей атома углерода
Гибридизацией орбиталей называют процесс, при котором орбитали, изначально имеющие разные формы и энергии смешиваются, образуя взамен такое же количество гибридных орбиталей, равных по форме и энергии.
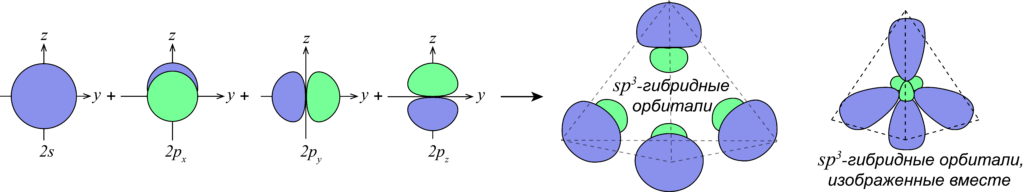
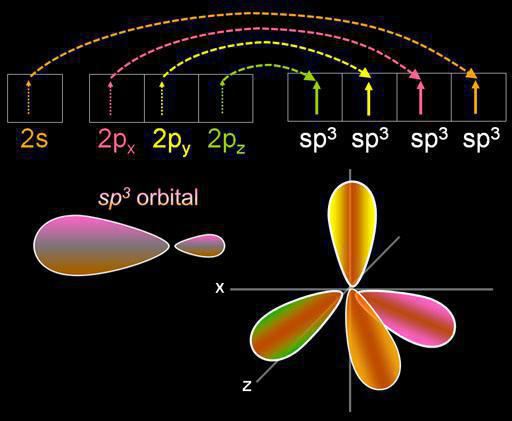
Так, например, при смешении одной s- и трех p-орбиталей образуются четыре sp3-гибридных орбитали:
В случае атомов углерода в гибридизации всегда принимает участие s-орбиталь, а количество p-орбиталей, которые могут принимать участие в гибридизации варьируется от одной до трех p-орбиталей.
Как определить тип гибридизации атома углерода в органической молекуле?
В зависимости от того, со скольким числом других атомов связан какой-либо атом углерода, он находится либо в состоянии sp3, либо в состоянии sp2, либо в состоянии sp-гибридизации:
| Количество атомов, с которыми связан атом углерода | Тип гибридизации атома углерода | Примеры веществ |
| 4 атома | sp3 | CH4 – метан |
| 3 атома | sp2 | H2C=CH2 – этилен |
| 2 атома | sp | HC≡CH — ацетилен |
Потренируемся определять тип гибридизации атомов углерода на примере следующей органической молекулы:
- Первый атом углерода связан с двумя другими атомами (1H и 1C), значит он находится в состоянии sp-гибридизации.
- Второй атом углерода связан с двумя атомами – sp-гибридизация
- Третий атом углерода связан с четырьмя другими атомами (два С и два Н) – sp3-гибридизация
- Четвертый атом углерода связан с тремя другими атомами (2О и 1С) – sp2-гибридизация.
Радикал. Функциональная группа
Под термином радикал, чаще всего подразумевают углеводородный радикал, являющийся остатком молекулы какого-либо углеводорода без одного атома водорода.
Название углеводородного радикала формируется, исходя из названия соответствующего ему углеводорода заменой суффикса –ан на суффикс –ил.
| Формула углеводорода | Название углеводорода | Формула радикала | Название радикала |
| CH4 | метан | -CH3 | метил |
| C2H6 | этан | -С2Н5 | этил |
| C3H8 | пропан | -С3Н7 | пропил |
| СnН2n+2 | …ан | -СnН2n+1 | … ил |
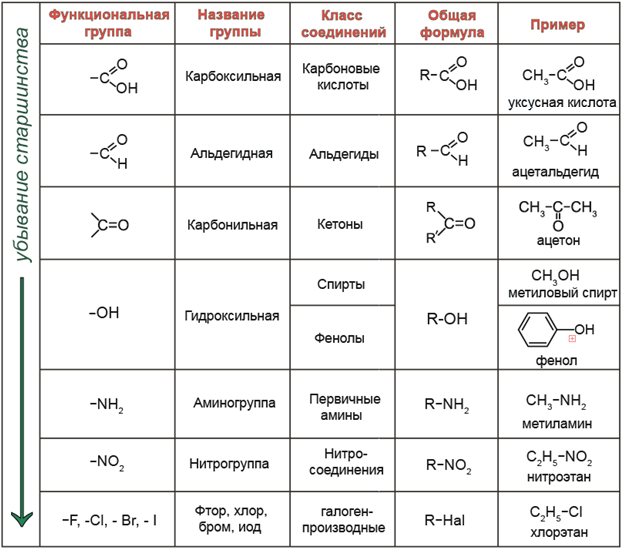
Функциональная группа — структурный фрагмент органической молекулы (некоторая группа атомов), который отвечает за её конкретные химические свойства.
В зависимости того, какая из функциональных групп в молекуле вещества является старшей, соединение относят к тому или иному классу.
R – обозначение углеводородного заместителя (радикала).
Радикалы могут содержать кратные связи, которые тоже можно рассматривать как функциональные группы, поскольку кратные связи вносят вклад в химические свойства вещества.
Если в молекуле органического вещества содержится две или более функциональных группы, такие соединения называют полифункциональными.
Гибридизация атомных орбиталей
14-Дек-2013 | Нет комментариев | Лолита Окольнова
В органической ( и неорганической химии мы часто встречаем понятие
Гибридизация атомных орбиталей
Гибридизация атомных орбиталей — гипотетический процесс смешения разных (s, p, d, f) орбиталей центрального атома многоатомной молекулы с возникновением одинаковых орбиталей, эквивалентных по своим характеристикам.
Обратите внимание на слово «гипотетический» — это значит предположительный, т.е. так химики попытались объяснить явление, когда атом образует большее количество связей, чем он может образовать в основном (невозбужденном) состоянии, когда есть определенное неспаренное число электронов.
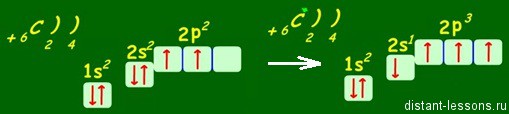
Например, возбужденное состояние атома углерода — основа органической химии:
Гибридизация атомных орбиталей происходит когда образуется ковалентная связь, и образуется она тогда, когда это энергетически более выгодно.
1 пример: смешение s- и двух p-орбиталей (2 другие остаются негибридными): Sp-гибридизация атомных орбиталей: молекула будет иметь линейную форму (180o) (у алкинов)
Примеры неорганических соединений: BeF2 (F-B-F) , CO2 (O=C=O), NO2+ (O=N+=O)
2 пример: смешение s- и трех p-орбиталей (одна p-орбиталь останется негибридной) : Sp2-гибридизация атомных орбиталей: молекула будет иметь треугольную форму (120o) (у алкенов)
Примеры неорганических соединений: BF3, ион NO3—, ион CO32-
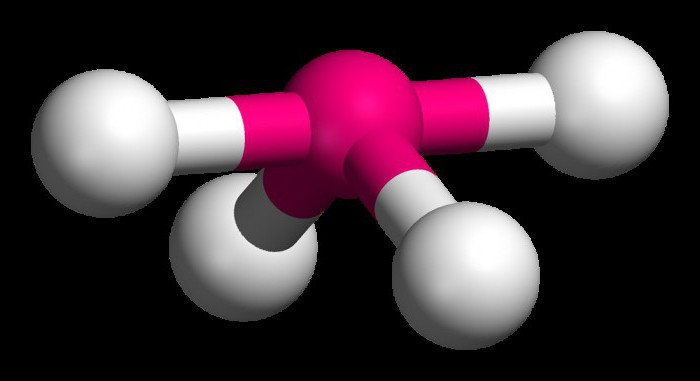
3 пример: смешение s- и четырех p-орбиталей: Sp3-гибридизация атомных орбиталей: молекула будет иметь тетраэдрическую форму (109,5o) (у алканов)
Примеры неорганических соединений: CH4, ион ClO4—, ион SO42-, ион NH4+
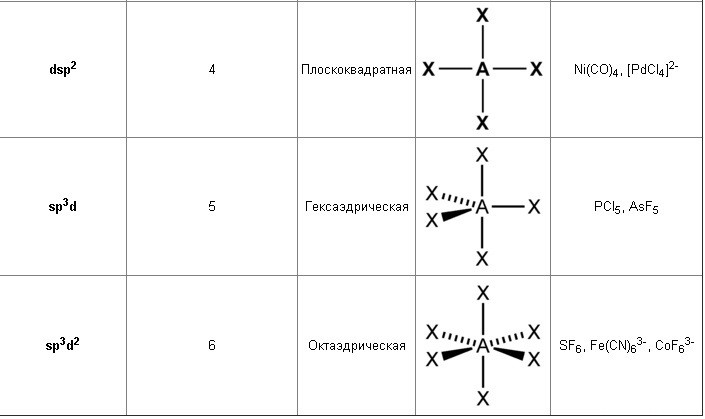
Возможна гибридизация атомных орбиталей, затрагивающая и d-орбиталь:
Чтобы определить тип гибридизации и форму химической частицы, поступают следующим образом:
- находят центральный атом и определяют число σ-связей (по числу концевых атомов);
- определяют степени окисления атомов в частице;
- составляют электронную конфигурацию центрального атома в нужной степени окисления;
- если это необходимо, проделывают то же самое для концевых атомов;
- изображают схему распределения валентных электронов центрального атома по орбиталям, при этом, вопреки правилу Гунда, максимально спаривают электроны;
- отмечают орбитали, участвующие в образовании связей с концевыми атомами;
- определяют тип гибридизации, учитывая все орбитали, участвующие в образовании связи, а также неподеленные электроны; если валентных орбиталей недостаточно, используют орбитали последующих энергетических уровней;
- по типу гибридизации определяют геометрию химической частицы.
Обсуждение: «Гибридизация атомных орбиталей»
(Правила комментирования)
Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа.
Типы связей в молекулах органических веществ
Одна из характеристик химических связей — тип перекрывания орбиталей атомов в молекуле.
По характеру перекрывания различают σ-(сигма) и π‑(пи) связи.
σ-Связь — это связь, в которой перекрывание орбиталей происходит вдоль оси, соединяющей ядра атомов.
σ-Связь может быть образована любыми типами орбиталей (s, p, d, гибридизованными).
σ-Связь — это основная связь в молекуле, которая преимущественно образуется между атомами.
Между двумя атомами возможна только одна σ-связь.
Виды σ-связей
π-Связь — это связь, в которой перекрывание орбиталей происходит в плоскости, перпендикулярной оси, соединяющей ядра атомов, сверху и снизу от оси связи.
π-Связь образуется при перекрывании только р- (или d) орбиталей, перпендикулярных линии связи и параллельных друг другу.
π-Связь является дополнительной к σ-связи, она менее прочная и легче разрывается при химических реакциях.
| Одинарная связь
С–С, С–Н, С–О |
Двойная связь
С=С, С=О |
Тройная связь
С≡С, С≡N |
| σ-связь | σ-связь + π-связь | σ-связь + две π-связи |
Гибридизация атомных орбиталей углерода
Электронная формула атома углерода в основном состоянии:
+6С 1s22s22p2
+6С 1s 2s
2p
В возбужденном состоянии: один электрон переходит с 2s-подуровня на 2р-подуровень.
+6С* 1s22s12p3
+6С* 1s2 2s1
2p3
Таким образом, в возбужденном состоянии углерод содержит четыре неспаренных электрона, может образовать четыре химические связи и проявляет валентность IV в соединениях.
При образовании четырех химических связей атомом углерода происходит гибридизация атомных орбиталей.
Гибридизация атомных орбиталей — это выравнивание электронной плотности атомных орбиталей разного типа с образованием новых, молекулярных орбиталей, форма и энергия которых одинаковы.
В гибридизацию вступают атомные орбитали с небольшой разницей в энергии (как правило, орбитали одного энергетического уровня). В зависимости от числа и типа орбиталей, участвующих в гибридизации, для атома углерода возможны sp3, sp2 и sp-гибридизация.
sp3-Гибридизация
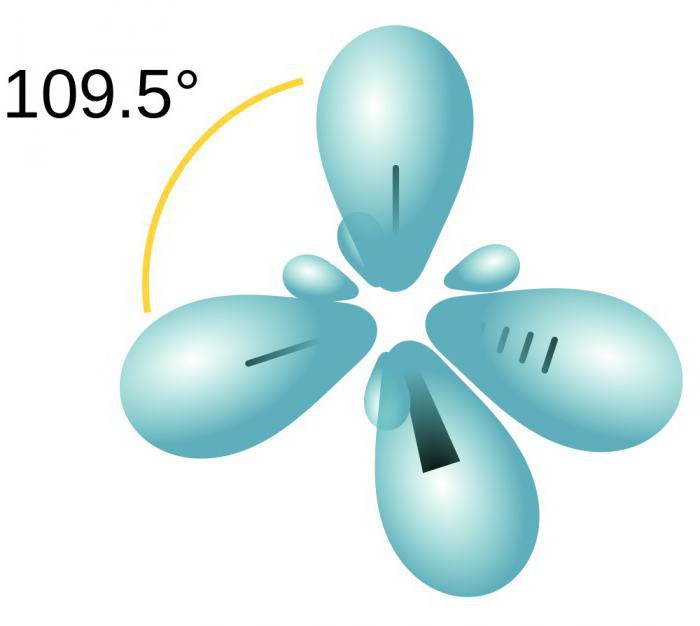
В sp3-гибридизацию вступают одна s-орбиталь и три p-орбитали. При этом образуются четыре sp3-гибридные орбитали:
Изображение с портала orgchem.ru
Четыре sp3-гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в состоянии sp3-гибридизации направлены в пространстве под углом 109о 28’ друг к другу, что соответствует тетраэдрическому строению.
Например, в молекуле метана CH4 атомы водорода располагаются в пространстве в вершинах тетраэдра, центром которого является атом углерода. Валентный угол Н–С–Н в метане равен 109о 28’
Молекулам линейных алканов с большим числом атомов углерода соответствует зигзагообразное расположение атомов углерода.
Например, пространственное строение н-бутана
sp2-Гибридизация
В sp2-гибридизацию вступают одна s-орбиталь и две p-орбитали. Одна p-орбиталь не гибридизуется:
Три sp2-гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому три sp2-гибридные орбитали атома углерода направлены в пространстве под углом 120о друг к другу, что соответствует плоскому строению (треугольник).
При этом негибридная р-орбиталь располагается перпендикулярно плоскости, в которой расположены три гибридные sp2— орбитали.
Изображение с портала orgchem.ru
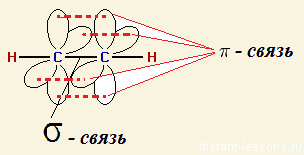
Например, молекула этилена C2H4 имеет плоское строение. Сигма-связь между атомами углерода образуется за счет перекрывания sp2-гибридных орбиталей. Пи-связь между атомами углерода образуется за счет перекрывания негибридных р-орбиталей.
Модель молекулы этилена:
sp-Гибридизация
В sp-гибридизацию вступают одна s-орбиталь и одна p-орбиталь. Две p-орбитали не вступают в гибридизацию:
Две sp-гибридные орбитали атома углерода направлены в пространстве под углом 180о друг к другу, что соответствует линейному строению.
Изображение с портала orgchem.ru
При этом две р-орбитали располагаются перпендикулярно друг другу и перпендикулярно линии, на которой расположены гибридные орбитали.
Например, молекула ацетилена имеет линейное строение.
Поговорим о том, как определить тип гибридизации, а также рассмотрим геометрическое строение молекулы.
История появления термина
В начале двадцатого века Л. Полинглом была предложена теория геометрии молекул с ковалентной связью. В качестве основы для образования связи было взято перекрывание электронных облаков. Метод стали называть валентными связями. Как определять тип гибридизации атомов в соединениях? Автор теории предлагал учитывать смешивание гибридных орбиталей.
Определение
Для того чтобы понять, как определить тип гибридизации в соединениях, разберем, что обозначает этот термин.
Гибридизация представляет собой смешивание электронных орбиталей. Данный процесс сопровождается распределением в них энергии, изменением их формы. В зависимости от того, в каком количестве будут смешиваться s- и p-орбитали, тип гибридизации может быть различным. В органических соединениях атом углерода может существовать в состоянии sp, sp2, sp3. Есть и более сложные формы, в которых участвуют, помимо sp, d-орбитали.
Правила выявления в молекулах неорганических веществ
Выявить вариант гибридизации можно для соединений с ковалентной химической связью, имеющих тип АВп. А – основной атом, В – лиганд, п – число от двух и выше. В подобной ситуации в гибридизацию будут вступать только валентные орбитали главного атома.
Способы определения
Поговорим подробнее о том, как определить тип гибридизации. В химическом понимании данный термин предполагает изменение энергии и формы орбиталей. Наблюдается подобный процесс в тех случаях, когда для образования связи используют электроны, которые принадлежат различным типам.
Чтобы понять, как определить тип гибридизации, рассмотрим молекулу метана. Данное вещество является первым представителем гомологического ряда насыщенных (предельных) углеводородов. В пространстве молекула СН4 является тетраэдром. Единственный атом углерода образует с водородами связи, сходные по энергии и длине. Для того чтобы образовались такие гибридные облака, используются три р- и один эс-электрон.
Четыре облака смешиваются, и возникает четыре одинаковых (гибридных) вида, имеющих форму неправильной восьмерки. Называют такой тип гибридизации sp3. Все углеводороды, в составе которых только простые (одинарные) связи, характеризуются именно таким типом гибридизации атома углерода. Валентный угол составляет 109 градусов 28 минут.
Продолжим разговор о том, как определить тип гибридизации. Примеры ненасыщенных углеводородов ряда этилена дают представление о sp2-гибридизации. Например, в молекуле этилена из четырех валентных электронов в образовании химической связи используется только три. Оставшийся негибридный р-электрон уходит на образование двойной связи.
Ацетилен является простейшим представителем класса СпН2п-2. Особенностью этого класса углеводородов является наличие тройной связи. Из четырех валентных электронов углеродного атома только два меняют свою форму и энергию, становясь гибридными. Два оставшихся электрона принимают участие в образовании двух двойных связей, определяя ненасыщенный характер этого класса органических соединений.
Заключение
Рассматривая вопрос, касающийся ковалентной химической связи для органических и для неорганических веществ, учитывают гибридизацию атомных орбиталей. При этом происходит выравнивание их энергии и формы. Электрон, располагающийся вблизи ядра связанного атома, характеризуется совокупностью орбиталей, которые обладают одинаковым квантовым числом. Информация о типе гибридизации дает возможность оценивать химические свойства вещества.