-
Чтобы найти парциальный объем газа необходимо сначала выразить его объемную долю в долях от единицы, а не в процентах, для чего нужно разделить ее (объемную долю) на 100. Затем нужно умножить общий объем газовой смеси на объемную долю конкретного газа.
V (газа) = φ (газа) * V (газовой смеси).
- Комментировать
- Жалоба
- Ссылка
Знаешь ответ на этот вопрос?
Сомневаешься в правильности ответа?
Получи верный ответ на вопрос 🏆 «Как найти объём газа из формулы: объёмная доля газа=V газа/V смеси х 100% …» по предмету 📕 Химия, используя встроенную систему поиска. Наша обширная база готовых ответов поможет тебе получить необходимые сведения!
Найти готовые ответы
Главная » Химия » Как найти объём газа из формулы: объёмная доля газа=V газа/V смеси х 100%
Расчеты массы (объема, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества
Для расчета массы (объема, количества вещества) продукта реакции, если данные по одному из веществ представлены в виде раствора с определенной массовой долей этого растворенного вещества, следует воспользоваться нижеследующим алгоритмом:
1) Прежде всего следует найти массу растворенного вещества. Возможны две ситуации:
* В условии даны масса раствора и массовая доля растворенного вещества (концентрация). В этом случае масса растворенного вещества рассчитывается по формуле:
* В условии даны объем раствора вещества, плотность этого раствора и массовая доля растворенного вещества в этом растворе. В таком случае следует воспользоваться формулой для расчета массы раствора:
После чего следует рассчитать массу растворенного вещества по формуле 1.
2) Рассчитать количество вещества (моль) участника реакции, масса которого стала известна из расчетов выше. Для этого воспользоваться формулой:
3) Записать уравнение реакции и убедиться в правильности расставленных коэффициентов.
4) Рассчитать количество моль интересующего участника реакции исходя из известного количества другого участника реакции, зная, что количества веществ любых двух участников реакции A и B относятся друг к другу как коэффициенты перед этими же веществами в уравнении реакции, то есть:
Если в условии требовалось рассчитать количество вещества, то действия на этом заканчиваются. Если же требуется найти его массу или объем, следует переходить к следующему пункту.
5) Зная количество вещества, определенное в п.4, мы можем рассчитать его массу по формуле:
Также, если вещество является газообразным и речь идет о нормальных условиях (н.у.), его объем может быть рассчитан по формуле:
Рассмотрим пару примеров расчетных задач по этой теме.
Пример 1
Рассчитайте массу осадка, который образуется при добавлении к 147 г 20%-ного раствора серной кислоты избытка раствора нитрата бария.
Решение:
1) Рассчитаем массу чистой серной кислоты:
m(H2SO4) = w(H2SO4) ∙ m(р-ра H2SO4)/100% = 147 г ∙ 20% /100% = 29,4 г
2) Рассчитаем количество вещества (моль) серной кислоты:
n(H2SO4) = m(H2SO4) / M(H2SO4) = 29,4 г/98 г/моль = 0,3 моль.
3) Запишем уравнение взаимодействия серной кислоты с нитратом бария:
H2SO4 + Ba(NO3)2 = BaSO4↓ + 2HNO3
4) В результате расчетов стало известно количество вещества серной кислоты. Осадок представляет собой сульфат бария. Зная, что:
n(BaSO4)/n(H2SO4) = k(BaSO4)/k(H2SO4), где n — количество вещества, а k — коэффициент в уравнении реакции,
можем записать:
n(BaSO4) = n(H2SO4) ∙ k(H2SO4)/k(BaSO4) = 0,3 моль ∙ 1/1 = 0,3 моль
5) Тогда масса осадка, т.е. сульфата бария, может быть рассчитана следующим образом:
m(BaSO4) = M(BaSO4) ∙ n(BaSO4) = 233 г/моль ∙ 0,3 моль = 69,9 г
Пример 2
Какой объем газа (н.у.) выделится при растворении необходимого количества сульфида железа (II) в 20%-ном растворе соляной кислоты с плотностью 1,1 г/мл и объемом 83 мл.
Решение:
1) Рассчитаем массу раствора соляной кислоты:
m(р-ра HCl) = V(р-ра HCl) ∙ ρ(р-ра HCl) = 83 мл ∙ 1,1 г/мл = 91,3 г
Далее рассчитаем массу чистого хлороводорода, входящего в состав кислоты:
m(HCl) = m(р-ра HCl) ∙ w(HCl)/100% = 91,3 г ∙ 20%/100% = 18,26 г
2) Рассчитаем количество вещества хлороводорода:
n(HCl) = m(HCl)/M(HCl) = 18,26 г/36,5 г/моль = 0,5 моль;
3) Запишем уравнение реакции сульфида железа (II) с соляной кислотой:
FeS + 2HCl = FeCl2 + H2S↑
4) Исходя из уравнения реакции следует, что количество прореагировавшей соляной кислоты с количеством выделившегося сероводорода связано соотношением:
n(HCl)/n(H2S) = 2/1, где 2 и 1 — коэффициенты перед HCl и и H2S соответственно
Следовательно:
n(H2S) = n(HCl)/2 = 0,5/2 = 0,25 моль
5) Объем любого газа, находящегося при нормальных условиях, можно рассчитать по формуле V(газа) = Vm ∙ n(газа), тогда:
V(H2S) = Vm ∙ n(H2S) = 22,4 л/моль ∙ 0,25 моль = 5,6 л
Автор: С.И. Широкопояс https://scienceforyou.ru/
Вычисление массы и объема газов
Если в условиях задачи указаны вещества в газообразном состоянии, то при вычислениях необходимо использовать газовые законы, связывающие количества и массы веществ с их объемами.
Задача 1. Вычислить объем диоксида углерода при н.у., взятого количеством
вещества 3 моль.
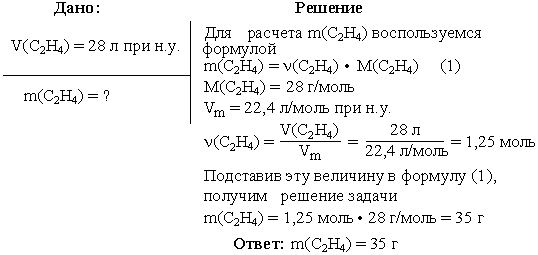
Задача 2. Вычислить массу этилена (C2H4), занимающего при н.у. объем 28 л.
Задача 3. Вычислить объемную долю метана в смеси, состоящей из 30 л
метана, 5 л этана и 2 л водорода. Объемы газов измерены при одинаковых
условиях.
Часто допускается ошибка, когда при проведении расчётов отождествляются величины массовых и объёмных долей вещества.
Чтобы показать ошибочность таких представлений, рассмотрим решение задачи, в которой расчёт объемов газов связан с вычислениями их масс.
Задача 4. Имеется газовая смесь, массовые доли газа в которой равны (%): метана – 65, водорода – 35. Определите объемные доли газов в этой смеси.
Таким образом, числовые значения массовых и объемных долей не совпадают.

Вовчик
В газовых смесях принято использовать термин «компоненты смеси», а не «примеси».
Для нахождения объёма нужно знать, в каких долях задаётся состав смеси — в объёмных или массовых. Общие формулы можно найти в литературе и Интернете; мы же будем рассматривать конкретную смесь — воздух. полагая для простоты, что он состоит только из кислорода и азота.
1) Состав задан в объёмных долях: rO2= 21%= 0,21; rN2= 79%= 0,79. mв = 1 кг. Н. у. Формула: Vв= mв/Mв* RT/p; Mв= rO2* MO2+ rN2*MN2= 0,21* 0,032+ 0,79* 0,028= 0,02884 кг/моль. Vв= 1/0,02884*8,314*273,15/(1,013* 10^5)= 0,777 м3.
2) Состав задан в массовых долях: gO2= 23%= 0,23; gN2= 77%= 0,77. Формула: Vв= (gO2/MO2+ gN2/MN2)* mвRT/p= (0,23/0,032+ 0,77/0,028)* 1* 8,314* 273,15/ (1,013* 10^5)= 0,778 м3. Получили почти один и тот же результат.
Компонентов в смеси будет больше — соответственно увеличится и число слагаемых в формулах.
- Курс
Меня зовут Быстрицкая Вера Васильевна.
Я репетитор по Химии
Вам нужны консультации по Химии по Skype?
Если да, подайте заявку. Стоимость договорная.
Чтобы закрыть это окно, нажмите «Нет».
НЕОБХОДИМЫЕ ТЕОРЕТИЧЕСКИЕ СВЕДЕНИЯ
КОЛИЧЕСТВО ВЕЩЕСТВА — отношение массы вещества к молярной массе вещества.
КОЛИЧЕСТВО ВЕЩЕСТВА — отношение объема газа к молярному объему (22,4л/моль). (н.у.)
МАССОВАЯ ДОЛЯ КОМПОНЕНТА В СМЕСИ — отношение массы компонента к массе всей смеси.
Обычно массовую долю выражают в %, но не обязательно.
МАССОВАЯ ДОЛЯ КОМПОНЕНТА В РАСТВОРЕ — отношение массы компонента к массе всего раствора.
Обычно массовую долю выражают в %, но не обязательно.
МОЛЬНАЯ ДОЛЯ КОМПОНЕНТА В СМЕСИ — отношение числа моль (количества вещества) компонента к суммарному числу моль всех веществ в смеси. Например, если в смесь входят вещества А, В и С, то:
ОБЪЕМНАЯ ДОЛЯ КОМПОНЕНТА В СМЕСИ (только для газов) — отношение объёма вещества А к общему объёму всей газовой смеси.
ОПРЕДЕЛЕНИЕ ВЫХОДА ПРОДУКТА по отношению к теоретически возможному :
АЛГОРИТМ 1
ВЫЧИСЛЕНИЕ МАССЫ ИЛИ ОБЪЕМА ВЕЩЕСТВА ПО ИЗВЕСТНОЙ МАССЕ ИЛИ ОБЪЕМУ ДРУГОГО ВЕЩЕСТВА, УЧАСТВУЮЩЕГО В РЕАКЦИИ
2. Записать уравнение реакции, расставим коэффициенты;
3. Найти молярные массы веществ, о которых идет речь в условии задачи
4. Найдем количество веществ, массы или объемы которых даны в условии задачи по формулам:
5. Над формулами веществ запишем найденные количества веществ, а под формулами — стехиометрические соотношения, отображаемые уравнением реакции
6. Составить соотношение количеств веществ (первая дробь — коэффициенты, равно, вторая дробь найденная величина, и что необходимо найти).
7. По формулам, указанным выше, найдем массу или объем вещества, которую требуется вычислить.
АЛГОРИТМ 2
ВЫЧИСЛЕНИЕ МАССЫ ПРОДУКТА ПО ИЗВЕСТНОЙ МАССЕ ИЛИ ОБЪЁМУ ИСХОДНОГО ВЕЩЕСТВА, СОДЕРЖАЩЕГО ПРИМЕСИ.
АЛГОРИТМ 2
ВЫЧИСЛЕНИЕ МАССЫ ИСХОДНОГО ВЕЩЕСТВА, СОДЕРЖАЩЕГО ПРИМЕСИ, ПО ИЗВЕСТНОЙ МАССЕ ИЛИ ОБЪЁМУ ПРОДУКТА РЕАКЦИИ
АЛГОРИТМ 3
ВЫЧИСЛЕНИЕ МАССЫ ПРОДУКТА ПО ИЗВЕСТНОЙ МАССЕ ИЛИ ОБЪЁМУ ИСХОДНОГО РАСТВОРА ВЕЩЕСТВА С ОПРЕДЕЛЕННОЙ МАССОВОЙ ДОЛЕЙ РАСТВОРЕННОГО ВЕЩЕСТВА
АЛГОРИТМ 4
ВЫЧИСЛЕНИЕ МАССЫ ПРОДУКТА РЕАКЦИИ ПО ИЗВЕСТНОЙ МАССЕ РЕАГЕНТА, ЕСЛИ ИЗВЕСТЕН ВЫХОД ПРОДУКТА РЕАКЦИИ.
АЛГОРИТМ 4
ВЫЧИСЛЕНИЕ МАССЫ ИСХОДНОГО ВЕЩЕСТВА ПО ИЗВЕСТНОЙ МАССЕ ПРОДУКТА РЕАКЦИИ, ЕСЛИ ИЗВЕСТЕН ВЫХОД ПРОДУКТА РЕАКЦИИ ОТ ТЕОРЕТИЧЕСКИ ВОЗМОЖНОГО.
АЛГОРИТМ 5
РАСЧЕТЫ ПО ХИМИЧЕСКИМ УРАВНЕНИЯМ, ЕСЛИ ОДНО ИЗ РЕАГИРУЮЩИХ ВЕЩЕСТВ ДАНО В ИЗБЫТКЕ.
26(Б) Задачи ЕГЭ ФИПИ 2015 на расчет массы вещества или объема газов


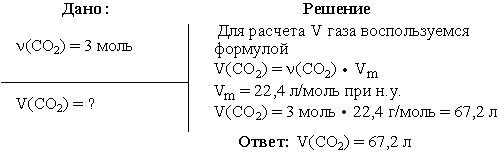


![[[pictureof]]](https://dist-tutor.info/s3/dist-tutor/user/20094/ava/thumbnails/mQ6siSVtAT1Szar.jpg)
























