|
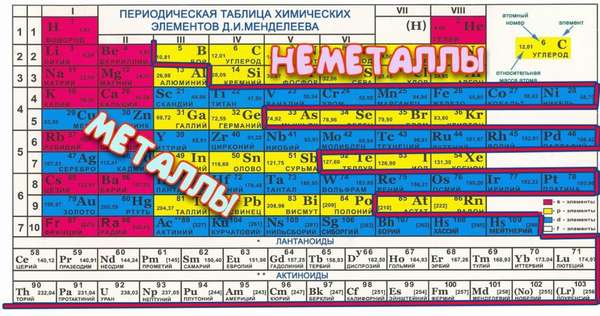
Где стоят металлы, а где неметаллы в таблице Менделеева? Можно ли как то их определить без запоминания? В таблице Менделеева существует два вида веществ — это металлы и не металлы. Не металлами в основном являются газы. Что бы определить металл это или не метал стоит знать что в правой стороне металлы, в левой не металлы. На это картинке показано где есть не металлы, выделены желтым и оранжевым, подчеркнутые синей линией, все остальное это металлы автор вопроса выбрал этот ответ лучшим wildcat 8 лет назад Со временем все неметаллы просто запоминаешь, тем более, что элементы эти всем хорошо известны, да и их количество невелико — всего 22. Но пока такой сноровки не приобретешь запомнить способ отделения металлов от неметаллов очень просто. Два последних столбца таблицы все целиком посвящены неметаллам — это крайний столбец инертных газов и начинаемый водородом столбец галогенов. В первых двух столбцах слева неметаллов вообще нет — там сплошные металлы. Начиная с третьей группы в столбцах появляются неметаллы — сперва один бор, потом в 4 группе уже два — углерод и кремний, в 5 группе — три — азот фосфор и мышьяк, в 6 группе неметаллов уже 4 — кислород, сера, селен и теллур, ну а далее следует уже группа галогенов про которую говорилось выше. Для облегчения запоминания неметаллов используется такая удобная таблица где все неметаллы стоят косынкой: Если в старом (сокращенном) варианте периодической таблицы провести прямую из левого верхнего угла к правому нижнему, то большинство неметаллов окажется вверху. Хотя и не все. И еще есть «полуметаллы», например, мышьяк и селен. Проще сказать, какие элементы неметаллы, потому что их значительно меньше металлов. И все они обычно выделены желтым как р-элементы (хотя и некоторые металлы туда попадают). В современном (длинном) варианте таблицы, с 18 группами, все неметаллы (кроме водорода) находятся справа. Это все газы, галогены, а также бор, углерод, кремний, фосфор и сера. Не так уж много. ольген 8 лет назад Металлы в таблице Д.И.Менделеева стоят во всех периодах, кроме 1-го (Н и Не), во всех группах, в побочных (В) подгруппах стоят только металлы (d-элементы). Неметаллы являются р-элементами и располагаются только в главных (А) подгруппах. Всего элементов-неметаллов 22 элемента и они располагаются ступеньками, начиная с ША группы, прибавляя по одному элементу в каждой группе: ША группа — В — бор, 1УА группа — С — углерод и Si — кремний; VA группа — азот (N), фосфор -Р, мышьяк — Аs; V1A группа (халькогены) — кислород (О), сера (S), селен (Sе), теллур (Те), V11A группа (галогены) — фтор (F ), хлор (Сl ), бром (Вr ), йод (I ), астат (Аt ); V111A группа инертные или благородные газы — гелий (Не), неон( Nе), аргон (Аr), криптон (Кr ), ксенон (Хе), радон (Rа). Водород располагается в первой (А) и седьмой(А) группах. Если провести мысленно диагональ от бериллия к борию, то сверху от диагонали в главных подгруппах располагаются неметаллы. Без запоминания и самой таблицы Менделеева запомнить, где металл и где неметалл — нереально. Но можно запомнить два простых правила. Первое правило — металлические свойства уменьшают в периоде слева направо. То есть, те вещества, что стоят вначале, являются металлами, в самом конце — неметаллы. Как раз первыми стоят щелочные и щелочно-земельные металлы, а затем все остальное, заканчиваясь инертными газами. Второе правило — металлические свойства растут сверху вниз по группе. Например, возьмем третью группу. Бор мы не назовем металлов, а вот под ним находится алюминий, который имеет выраженные металлические свойства. Марлена 6 лет назад Я помню как в школе преподаватель разделял линейкой таблицу Менделеева и показывал нам территории металлов и неметаллов. Таблица Менделеева делится на две зоны по диагонали. Все выше кремния и бора — это неметаллы. Также в новых таблицах эти две группы отмечены разными цветами. moreljuba 6 лет назад Специально для вас и для того чтобы вы наглядно смогли понять как же можно легко различить металлы и не металлы в таблице, привожу вам вот такую схему: Красным маркером выделена разделяющая черта металлы от неметаллов. Прочертите так на своей табличке и всегда будете знать. IsaacP 6 лет назад Нас в школе учили разделять линейкой таблицу Менделеева по диагонали, начиная с Бора и заканчивая Астатом, это и былитерритории металлов и неметаллов. Все выше кремния и бора — это неметаллы. Лично я пользуюсь такой таблицей переодических элементов. Andrey U 6 лет назад Как узнать металл или не металл, металл всегда находится в твердом состоянии, кроме ртути, а не металл может быть в любой форме, мягкий, твердой, жидкой, и так далее. Так же можно определять по цвету, как уже стало понятно металл, металлического цвета. Как определить его в таблице Менделеева, для этого надо провести диагональную линию от бора до астата, и все те элементы которые выше линии относятся к не металлу, а те что ниже линии к металлу. Помощни к 6 лет назад Периодическая таблица Менделеева более информативна, чем может показаться с первого взгляда. В ней можно узнать о элементе металл он или неметалл. Для этого нужно уметь визуально разделять таблицу на две части: То, что под красной чертой, это металлы, остальные элементы — это неметаллы. Знаете ответ? |
План урока:
Физические свойства металлов
Физические свойства неметаллов
Способы получения металлов
Химические свойства металлов
Способы получения неметаллов
Химические свойства неметаллов
Коррозия металла
Биологическая роль металлов и неметаллов
Применение металлов и неметаллов
Физические свойства металлов
Металлы – химические элементы, атомы которых в процессе реакции стремятся отдавать электроны. Они обладают металлической кристаллической решеткой и общими физическими свойствами. На данный момент известно более 87 металлов.
Для металлов характерен ряд свойств:
- твердость (кроме ртути, которая представляет собой жидкость);
- металлический блеск;
- проводимость электрического тока и тепла;
- пластичность.
Металлы при ударах не разрушаются, а меняют форму. С этой особенностью связано то, что из них производят проволоку, металлические листы и др. Развитие бронзового и железного века связано с производством товаров из металлов.
Физические свойства неметаллов
Неметаллы – химические элементы, атомы которых стремятся принять чужие электроны. Для них характерны атомные и молекулярные кристаллические решетки. Для атомов неметаллов не характерны общие физические свойства. На данный момент существует 22 неметалла.
Для неметаллов характерен ряд свойств:
- хрупкость (неметаллы нельзя ковать);
- отсутствие блеска;
- непроводимость электрического тока и тепла.
Расположение металлов и неметаллов в периодической таблице Д.И. Менделеева
Определить, является простое вещество металлом или неметаллом, можно с помощью периодической таблицы Менделеева. Металлы располагаются ниже диагонали «водород-бор- кремний-мышьяк-теллур-астат», а неметаллы выше.
Красные ячейки – неметаллы, синие – металлы
Элементы, расположенные вблизи диагонали, обладают смешанными свойствами: проявляют как металлические, так и неметаллические свойства. Они называются полуметаллами.
Красные ячейки – полуметаллы
Полуметаллы имеют ковалентную кристаллическую решетку при наличии металлической проводимости (электропроводности). Валентных электронов у них либо недостаточно для образования полноценной ковалентной связи, либо они не удерживаются достаточно прочно из-за больших размеров атома. Поэтому связь в ковалентных кристаллах этих элементов имеет частично металлический характер.
Закономерности в таблице Д.И. Менделеева
Каждый атом состоит из протонов, нейтронов и электронов. Протоны и нейтроны находятся в ядре, который несет положительный заряд. Вокруг ядра движутся отрицательно заряженные электроны. Атомный номер указывает на количество протонов.
Чем больше заряд ядра, тем сильнее к нему притягиваются электроны. Т.о., атому сложнее отдавать электроны. Поэтому в периоде слева направо, с увеличением порядкового номера металлические свойства ослабевают, а неметаллические – усиливаются.
Неметаллы стремятся принять электроны от других атомов. Период в таблице указывает на количество электронных уровней. По мере увеличения числа орбиталей электроны отдаляются от ядра и атому сложнее удерживать электроны на последних уровнях. Т.о., в группе сверху вниз количество орбиталей возрастает, поэтому металлические свойства усиливаются, а неметаллические – уменьшаются.
Способы получения металлов
Большую часть металлов получают из оксидов при нагревании.
Fe2O3 + 3 CO →2 Fe + 3 CO2
MnO2 + 2 C → Mn + CO2
Металлы, имеющие на внешнем уровне один-два электрона, получают с помощью электролиза расплавов.
NaCl → Na+ + Cl—
Химические свойства металлов
Все металлы проявляют восстановительные свойства. Легкость в отдачи внешнего электрона применяется в фотоэлементах. Степень активности определяется рядом активности. У самых активных на внешнем уровне располагается по одному электрону.
Общие химические свойства металлов выражаются в реакциях со следующими соединениями.
- С неметаллами
4 Li + O2→ 2 LiO2
3 Mg + N2 → Mg3N2
Активные металлы реагируют с галогенами и кислородом. С азотом взаимодействуют только литий, кальций и магний. Большинство металлов при взаимодействии с кислородом образуют оксиды, а наиболее активные металлы – пероксиды (N2O2).
- С оксидами металлов
2 Ca + MnO2 → 2 CaO + Mn(нагревание)
- С кислотами
Mg + H2SO4(разб)→MgSO4 + H2
Водород в кислотах вытесняют только те металлы, которые в ряду напряжений стоят до водорода.
- С растворами солей
Fe + CuSO4→ Cu + FeSO4
Cu + 2 AgNO3→ 2 Ag + Cu(NO3)2
Более активные металлы вытесняют из соединений менее активные.
- Химические свойства щелочных и щелочно-земельных металлов (реакции с водой)
2 Na + 2 H2O → 2 NaOH + H2
Ca + 2 H2O →Ca(OH)2 + H2
Способы получения неметаллов
Неметаллы синтезируют из природных соединений с помощью электролиза.
2 KCl → 2 K + Cl2
Также неметаллы получают в результате окислительно-восстановительных реакций.
SiO2 + 2 Mg → 2 MgO + Si
Химические свойства неметаллов
Неметаллы проявляют окислительные свойства. Самый активный неметалл – фтор. Он бурно реагирует со всеми веществами, а некоторые реакции сопровождаются горением и взрывом. В атмосфере фтора горят даже вода и платина. Фтор окисляет кислород и образует фторид кислорода OF2.
Неметаллы вступают в реакции со следующими веществами.
- С металлами
3 F + 2 Al → 2 AlF3 (нагревание)
S + Fe →FeS (нагревание)
- С другими неметаллами
2 F2 + C → CF2 (нагревание)
S + O2→ SO2(нагревание)
- Со сложными веществами
4 F2 + CH4→CH3F + HF
3 O2 + 4 NH3→ 2 N2 + 6 H2O
Меньшей активностью обладают такие неметаллы как бор, графит, алмаз. Они могут проявлять восстановительные свойства.
2 C + MnO2 → Mn + 2 CO
4 H2 + Fe3O2 → 3 Fe + 4 H2O
Коррозия металла
Коррозия – это процесс разрушения металлов или металлических конструкций под действием кислорода, воды и вредных примесей. Не все металлы подвергаются коррозии. Их стойкость зависит от ряда факторов.
- На благородных металлах не образуется коррозия.
- На поверхности алюминия, титана, цинке, хрома и никеля есть оксидная пленка, которая предотвращает процессы коррозии.
Различают несколько видов коррозии – химическую и электрохимическую.
Химическая коррозия
Химическая коррозия сопровождается химическими реакциями. Она образуется под действием газов.
3 Fe + 2 O2 → Fe3O4
2 Fe + 3 Cl2 → 2 FeCl3
Электрохимическая коррозия
Электрохимическая коррозия – процесс разрушения металлов или металлических конструкций, который сопровождается электрохимическими реакциями. В большинстве металлов находятся примеси. В процессе коррозии электродами могут служить не только металлы, но и его примеси.
Например, в железе могут находиться примеси олова. В этом случае на аноде электроны переносятся от олова к железу и металлы растворяются, т.е. железо подвергаются коррозии. На катоде восстанавливается водород из воды или растворенного кислорода. Электрохимическая коррозия может сопровождаться следующими процессами.
Анод: Fe2+ — 2e → Fe0
Катод: 2H+ + 2e → H2
Способы защиты от коррозии
В промышленности популярны различные методы защиты металлов от коррозии.
- Защитные покрытия
Покрытия защищают поверхности от действия окислителей. Ими служат различные вещества:
- покрытие менее активным металлом (железо покрывают оловом);
- краски, лаки, смазки.
- Создание специальных сплавов
Физические свойства сплавов и чистых металлов отличаются. Поэтому для повышения стойкости в сплав необходимо добавить дополнительные металлы.
Биологическая роль металлов и неметаллов
В организмах содержится множество различных металлов и неметаллов. Различных химических элементов в организме может не хватать, поэтому приходится потреблять их извне.Химические элементы можно разделить на две большие группы – макроэлементы и микроэлементы.
К макроэлементам относятся вещества, содержание которых в организме превышает 0,005 %. Эта группа включает водород, углерод, кислород, азот, натрий, магний, фосфор, сера, хлор, калий, кальций.Микроэлементы – элементы, содержание которых не превышает 0,005%. К ним относятся железо, медь, селен, йод, хром, цинк, фтор, марганец, кобальт, молибден, кремний, бром, ванадий, бор. Каждый макро- и микроэлемент в организме выполняет определенную функцию.
Применение металлов и неметаллов
В синтезе химических препаратов и лекарств применяются чистые металлы и неметаллы. В органической химии металлы используются в качестве катализаторов, а также при получении металлорганических соединений. Неметаллы служат исходным сырьем для получения чистых кислот и других химических соединений.
Статьи
Основное общее образование
Линия УМК В. В. Лунина. Вводный курс (7)
Линия УМК В. В. Лунина. Химия (8-9)
Химия
Неметаллы. Физические и химические свойства
Неметаллы – вещества, обладающие неметаллическими свойствами и находящиеся в правом верхнем углу таблицы Менделеева. Открытие неметаллов произошло сравнительно недавно, в отличии от металлов, которые издавна известны человеку. В настоящее время открыто 22 неметаллических элемента.
11 апреля 2019
Положение неметаллов в периодической системе
Как же определить, относится вещество к металлам или к неметаллам?
Если внимательно посмотреть на Периодическую систему Д.И. Менделеева (подробно с классификацией элементов знакомимся в параграфе 42 учебника по химии для 8 класса под редакцией Еремина В.В.) и провести условную диагональ от водорода через бор до астата и неоткрытого пока элемента № 118, таблица неметаллов займет правый верхний угол.
Каждый горизонтальный период таблицы заканчивается элементом с завершенным внешним энергетическим уровнем. Эта группа элементов носит название благородные газы и имеет особые свойства, с которыми можно познакомиться в параграфе 18 учебника «Химия» для 8 класса под редакцией Еремина В.В.
При рассмотрении электронного строения неметаллов можно заметить, что энергетические уровни атома заполнены электронами больше чем на 50% (исключение – бор), и у элементов, расположенных в таблице справа налево количество электронов на внешнем уровне увеличивается. Поэтому в химических реакциях эта группа веществ может быть как акцептором электронов с окислительными свойствами, так и донором электронов с восстановительными свойствами.
Вещества, образующие диагональ бор-кремний-германий-мышьяк-теллур, являются уникальными, и в зависимости от реакции и реагента могут проявлять как металлические, так и неметаллические свойства. Их называют металлоиды. В химических реакциях они проявляют преимущественно восстановительные свойства.

Химия. Базовый уровень. 10 класс. Учебник.
Учебник написан преподавателями химического факультета МГУ им. М. В. Ломоносова. Простота и доступность изложения курса органической химии , большое количество иллюстраций , а также разнообразные вопросы упражнения и задачи способствуют успешному усвоению учебного материала. Учебник соответствует Федеральному государственному образовательному стандарту среднего общего образования.
Купить
Физические свойства неметаллов. Аллотропия
Если смотреть на металлы, то невооруженным глазом можно заметить общие свойства — металлический блеск, твердое агрегатное состояние (исключение — жидкая ртуть), тепло- и электропроводность.
С неметаллами все намного сложнее. Они могут иметь молекулярное и немолекулярное строение. Благодаря различиям в строении, простые вещества неметаллы существуют в трех агрегатных состояниях:
- Молекулярные:
- Летучие, газообразные, бесцветные кислород, водород.
- Газообразные, окрашенные хлор, азот, фтор.
- Единственный жидкий представитель — темно-красный бром.
- Твердые, но хрупкие вещества с невысокой температурой плавления — кристаллы йода, серы, белого фосфора.
- Немолекулярные:
- Твердые вещества с высокой температурой плавления — кремний, графит, алмаз и красный фосфор.
Большинство из неметаллических веществ плохо проводят электричество и тепло.
Исключением является графит — разновидность углерода.
Аллотропия — уникальная способность неметаллического элемента образовывать несколько простых веществ. В естественной среде существуют аллотропные модификации элементов, которые отличаются физическими и химическими свойствами. К ним относятся озон и кислород, графит и алмаз. Подробнее о физических свойствах неметаллов вы можете узнать в учебнике «Химия. 9 класс».
Химические свойства неметаллов
Как мы разобрали выше, группа неметаллов довольно полиморфна и в зависимости от типа реакций, в которых они участвуют, могут проявлять и окислительные, и восстановительные свойства. Фтор — исключение в этом ряду. Он всегда окислитель.
В ряду F,O,N,CL,Br,I,S,C,Se,P,As,Si,H окислительные свойства уменьшаются. Восстановительные свойства кислород может проявлять только в отношении фтора.
- Реакции с металлами.
В этом типе реакций проявляются окислительные свойства и неметаллы принимают электроны с образованием отрицательно заряженных частиц.
Са + Сl2 = СаСl2
Са + O2 = СаO2
Na + Сl2 = Na+Сl2
- Реакции с водородом
Практически все неметаллы реагируют с водородом. Лишь благородные газы составляют исключение для реакций данного типа. Продуктом реакции являются летучие водородные соединения:
Cl2 + H2 = 2HCl
С + 2Н2 = СН4
- Реакции с кислородом.
Неметаллы образуют кислотные или несолеобразующие оксиды.
S + O2 = SO2
P + 5O2 = 2P2O5
4. Взаимодействие с водой и кислотами для неметаллов не характерно.
Что ещё почитать?
ОГЭ по химии — 2019: расписание, критерии оценивания, типы заданий
Биография Д.И. Менделеева. Интересные факты из жизни великого химика
Карбоновые кислоты
Массовая доля вещества
История открытия неметаллов
Медная посуда, железные орудия труда, золотые украшения — издавна человек замечал, что у всех этих веществ есть определенные общие свойства:
- они проводят тепло и электрический ток;
- для них характерен металлический блеск;
- благодаря пластичности и ковкости им можно придать любую форму;
- для всех веществ характерна металлическая кристаллическая решетка.
В противовес металлам были и другие вещества, не обладающие металлическими свойствами, и названные соответственно неметаллами. Практически до конца XVII века ученым-алхимикам было известно всего лишь два вещества-неметалла — углерод и сера.
В 1669 году Бранд в поисках «философского камня» открыл белый фосфор. И за короткий период с 1748 по 1798 годы было открыто около 15 новых металлов и 5 неметаллов.
Попытки открытия фтора стоили исследователям не только здоровья, но и жизни. Деви, братья Кнокс, Гей-Люссак — это неполный список жертв науки, что потеряли здоровье в попытках выделить фтор из плавикового шпата. Лишь в 1886 году Муассан решил сложную задачу способом электролиза. И получил первый галоген, а ещё – ядовитый хлор. Во времена Первой мировой войны его использовали как оружие массового поражения.
В настоящее время открыто 22 неметаллических элемента.
#ADVERTISING_INSERT#
Дмитрий Менделеев смог создать уникальную таблицу химических элементов, главным достоинством которой была периодичность. Металлы и неметаллы в таблице Менделеева располагаются так, что их свойства изменяются периодическим образом.
Периодическая таблица Менделеева

Создание данной структурированной системы бесценно для науки и для человечества в целом. Именно это открытие дало толчок развитию всей химии на долгие годы.
Интересно знать! Существует легенда, что готовая система привиделась ученому во сне.
В интервью одному журналисту ученый объяснил, что работал над ней 25 лет и то, что она ему снилась – вполне естественно, но это не значит, что во сне пришли все ответы.
Созданная Менделеевым система делится на две части:
- периоды – столбики по горизонтали в одну или две строки (ряды),
- группы – вертикальные строчки, в один ряд.
Всего в системе 7 периодов, каждый следующий элемент отличен от предыдущего большим количеством электронов в ядре, т.е. заряд ядра каждого правого показателя больше левого на единицу. Каждый период начинается с металла, а заканчивается инертным газом – именно это и есть периодичность таблицы, ведь свойства соединений меняются внутри одного периода и повторяются в следующем. При этом, следует помнить, что 1-3 периоды неполные или малые, в них всего 2, 8 и 8 представителей. В полном периоде (т.е. оставшихся четырех) по 18 химических представителей.

Для облегчения поиска группы имеют свое название, а металлические свойства субстанций усиливаются с каждой нижней строчкой, т.е. чем ниже соединение, тем больше у него будет атомных орбит и тем слабее электронные связи. Также меняется и кристаллическая решетка – она становится ярко выраженной у элементов с большим количеством атомных орбит.
В химии используют три вида таблиц:
- Короткая – актиноиды и лантаноиды вынесены за границы основного поля, а 4 и все последующие периоды занимают по 2 строчки.
- Длинная – в ней актиноиды и лантаноиды вынесены за границу основного поля.
- Сверхдлинная – каждый период занимает ровно 1 строку.
Главной считается та таблица Менделеева, которая была принята и подтверждена официально, но для удобства чаще используют короткую версию. Металлы и неметаллы в таблице Менделеева располагаются согласно строгим правилам, которые облегчают работу с ней.
Это интересно! Уроки химии: катионы и анионы – что это такое

- пластичность,
- электропроводимость,
- блеск,
- легкая отдача электронов,
- ковкость,
- теплопроводность,
- твердость (кроме ртути).
Из-за различной химической и физической сути свойства могут существенно отличаться у двух представителей этой группы, не все они похожи на типичные природные сплавы, к примеру, ртуть – это жидкая субстанция, но относится к данной группе.

Некоторые элементы такого типа могут существовать только доли секунды, а некоторые не встречаются в природе совсем – их создали в искусственных условиях лаборатории. У каждой из групп металлов в системе есть свое название и признаки, которые отличают их от других групп.
Это интересно! Уроки химии: что это такое галогены
При этом отличия у них весьма существенные. В периодической системе все металлы располагаются по количеству электронов в ядре, т.е. по увеличению атомной массы. При этом для них характерно периодическое изменение характерных свойств. Из-за этого в таблице они не размещаются аккуратно, а могут стоять неправильно.
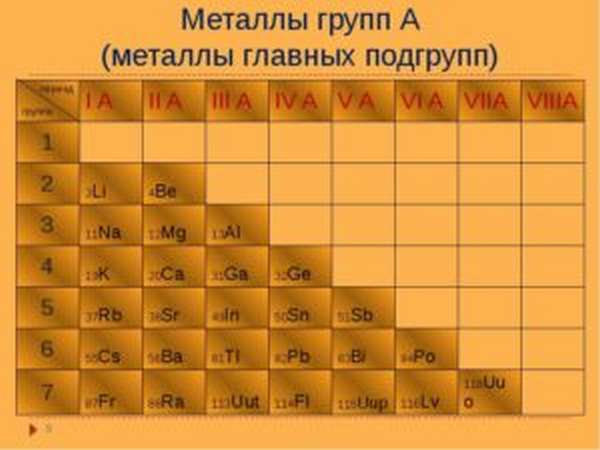
Как отличить металл от неметалла?
Как определить металл в соединении? Существует простой способ определения, но для этого необходимо иметь линейку и таблицу Менделеева. Для определения надо:
- Провести условную линию по местам соединения элементов от Бора до Полония (можно до Астата).
- Все материалы, которые будут слева линии и в побочных подгруппах – металл.
- Вещества справа – другого типа.
Это интересно! Что такое алканы: строение и химические свойства
Однако у способа есть изъян – он не включает в группу Германий и Сурьму и работает только в длинной таблице. Метод можно использовать в качестве шпаргалки, но чтобы точно определить вещество, следует запомнить список всех неметаллов. Сколько их всего? Мало – всего 22 вещества.
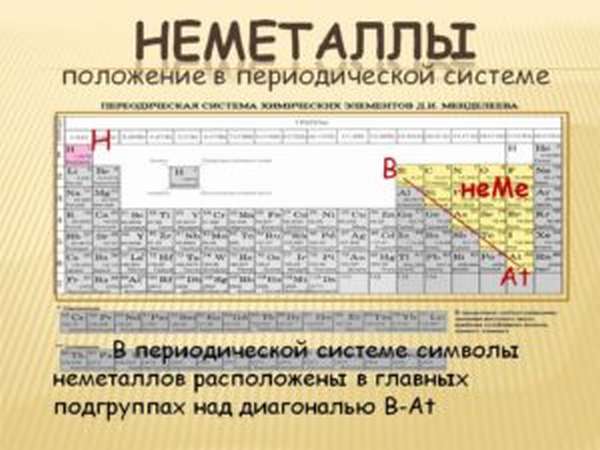
- При комнатной температуре – твердые, за исключением ртути. При этом они блестят и хорошо проводят электрический ток.
- У них на внешнем уровне ядра меньшее количество атомов.
- Состоят из кристаллической решетки (кроме ртути), а все другие элементы имеют молекулярную или ионную структуру.
- В периодической системе все неметаллы – красного цвета, металлы – черного и зеленого.
- Если двигаться слева направо в периоде, то заряд ядра вещества будет увеличиваться.
- У некоторых веществ свойства выражены слабо, но они все равно имеют характерные признаки. Такие элементы относятся к полуметаллам, например Полоний или Сурьма, они обычно располагаются на границе двух групп.
Внимание! В левой нижней части блока в системе всегда стоят типичные металлы, а в правой верхней типичные газы и жидкости.
Важно запомнить, что при перемещении в таблице сверху вниз становятся сильнее неметаллические свойства веществ, поскольку там располагаются элементы, которые имеют отдаленные внешние оболочки. Их ядро отделено от электронов и поэтому они притягиваются слабее.
Полезное видео
Подведем итоги
Отличить элементы будет просто, если знать основные принципы формирования таблицы Менделеева и свойства металлов. Полезно будет также запомнить и список остальных 22 элементов. Но не нужно забывать, что любой элемент в соединении следует рассматривать в отдельности, не учитывая его связей с другими веществами.
Содержание
- — Как определить металлы и неметаллы в химии?
- — Где находятся неметаллы в таблице?
- — Где расположены элементы металлы в таблице Менделеева?
- — Какие есть металлы в таблице Менделеева?
- — Какие вещества называют неметаллами?
- — Что означает цвет элемента в таблице Менделеева?
- — В каком виде встречаются Неметаллы в природе приведите примеры?
- — Какие элементы относятся к Неметаллам где они расположены в периодической системе?
- — Где расположены элементы неметаллы в Псхэ?
- — Где в основном располагаются металлы в Псхэ?
- — Где расположены атомы металлов?
- — В каком виде металлы находятся в природе?
- — Какие химические элементы относятся к металлам?
- — Сколько групп в периодической системе?
- — Какое строение имеют металлы?
В нашей периодической таблице символы неметаллов красные, а металлов – синие. Если провести диагональ примерно из левого верхнего угла в правый нижний, то элементы главных подгрупп выше диагонали будут неметаллами, а ниже – металлами.
Как определить металлы и неметаллы в химии?
Определить, является простое вещество металлом или неметаллом, можно с помощью периодической таблицы. Химические элементы металлы, образующие простые вещества с металлическими свойствами, располагаются в периодической таблице слева ниже диагонали «водород — бор — кремний — мышьяк — теллур — астат — № 118».
Где находятся неметаллы в таблице?
Менделеева Если в Периодической системе провести диагональ от бериллия к астату, то справа вверх по диагонали будут находиться элементы-неметаллы, а слева снизу – металлы, к ним же относятся элементы всех побочных подгрупп, лантаноиды и актиноиды.
Где расположены элементы металлы в таблице Менделеева?
В Периодической системе химических элементов Д. И. Менделеева металлы располагаются ниже диагонали бериллий – астат. Элементы, расположенные вблизи диагонали, например, бериллий, алюминий, титан, германий, сурьма обладают двойственным характером и относятся к металлоидам.
Какие есть металлы в таблице Менделеева?
Таблица «Металлы»
| Группа металлов | Металл |
|---|---|
| постпереходные | алюминий, свинец, олово и т.д. |
| Тугоплавкие | молибден, вольфрам |
| Цветные | медь, титан, магний и т.д. |
| Благородные | золото, серебро и т.д. |
Какие вещества называют неметаллами?
Немета́ллы — химические элементы с типично неметаллическими свойствами, которые занимают правый верхний угол Периодической системы. Курсивом выделены металлоиды, чьи свойства близки к металлам. В отличие от металлов, неметаллов гораздо меньше, всего их насчитывается 22 элемента.
Что означает цвет элемента в таблице Менделеева?
Как правило, разными цветами в таблице Менделеева обознаются s-, p-, d- и f-семейства. Например, s-семейство означает, что у этих элементов последним заполняется энергетический подуровень S. У p-семейства — подуровень p соответственно. Встречаются также таблицы, где разными цветами обознаются металлы и неметаллы.
В каком виде встречаются Неметаллы в природе приведите примеры?
В свободном виде в природе встречаются благородные газы, кислород, азот, сера, углерод, мышьяк. Часть неметаллов встречается в природе в виде соединений, в которых проявляет только положительные степени окисления. К ним относятся фосфор, кремний, германий, бор и некоторые другие.
Какие элементы относятся к Неметаллам где они расположены в периодической системе?
К неметаллическим элементам относятся p-элементы, а также водород и гелий, которые в свою очередь относятся к s-элементам. Они расположены правее и выше диагонали бор-астат. Всего же известно 22 неметалла.
Где расположены элементы неметаллы в Псхэ?
Неметаллы в периодической системе расположены в начале главных подгрупп, начиная с третьей группы и конце периодов, т. е. в правой верхней части периодической системы.
Где в основном располагаются металлы в Псхэ?
В периодической системе Менделеева металлы расположены ниже диагонали бор-астат. Т. е. это представители I-III групп (главных подгрупп, начиная со второго периода) и все представители побочных подгрупп.
Где расположены атомы металлов?
Строение атомов металлов определяет их положение в периодической системе химических элементов Д. И. Менделеева. … Следовательно, элементы-металлы А-групп расположены слева внизу от условной диагонали, проведённой от бора к астату.
В каком виде металлы находятся в природе?
Вследствие высокой активности большинство металлов находится в природе в виде соединений. Лишь немногие встречаются в самородном состоянии: Au, Ag, Pt, Hg, Cu (в песчаных россыпях, в жильных образованиях горных пород и т. д.). Химический состав руд чрезвычайно разнообразен.
Какие химические элементы относятся к металлам?
Некоторые группы/семейства металлов (по разным классификациям)
- Щелочные (например: Литий, Натрий, Калий)
- Щёлочноземельные (например: Кальций, Стронций, Барий) …
- Переходные (например: Уран, Титан, Железо, Никель, Кобальт, Молибден, Вольфрам, Платина)
- Постпереходные:
Сколько групп в периодической системе?
Современная форма Периодической системы химических элементов (в 1989 году Международным союзом теоретической и прикладной химии рекомендована длинная форма таблицы) состоит из семи периодов (горизонтальных последовательностей элементов, расположенных по возрастанию порядкового номера) и 18 групп (вертикальных …
Какое строение имеют металлы?
Металлы имеют кристаллическое строение. Оно характеризуется закономерным расположением атомов в пространстве и образованием кристаллической решетки. Типы кристаллических решеток. Кристаллическое строение металлов условно можно представить как упорядоченное расположение атомов в пространстве.
Интересные материалы:
Для чего используется лоратадин?
Для чего используется тире?
Для чего используется центр обеспечения безопасности Windows?
Для чего используют Биндер?
Для чего используют Фритюрное масло?
Для чего используют изопропиловый спирт?
Для чего используют цветки календулы?
Для чего капли Нормакс?
Для чего кнопка на катушке?
Для чего коньяк в тесте?