Дьюи Б. Ларсон — Структура физической вселенной (том 2)
Глава 2: Межатомные расстояния
Уравнение 1 – 10 указывает, что расстояние между любыми двумя атомами в
твердой совокупности – функция определенных вращений атомов. Поскольку
каждый атом способен принимать любое из нескольких разных относительных
ориентаций вращательных движений, из этого следует, что для каждой
комбинации атомов имеется ряд определенных возможных вращений. Число
возможных альтернатив увеличивается за счет двух дополнительных
факторов, которые уже обсуждались. Как отмечалось в главе 10 тома 1,
атом обладает вариантом вращения с обычным магнитным смещением и
положительным электрическим смещением или со следующим более высоким
магнитным смещением и отрицательным электрическим приращением. В любом
случае, действующую величину, удельное вращение, можно изменить
расширением движения на вторую единицу вибрации, как говорилось в главе
1.
При надлежащих условиях, можно реально осознавать каждый из многих
вариантов величины удельного вращения и соответствующие величины
межатомных расстояний. Но в любом конкретном наборе обстоятельств, одни
комбинации вращений более вероятны, чем другие. В обычной практике число
разных величин расстояния между одними и теми же двумя атомами
относительно невелико, кроме каких-то особых случаев. Сейчас дела
обстоят так, что из теоретических допущений мы можем вычислить небольшой
набор вероятных межатомных расстояний для каждого элемента и соединения.
Бесспорно, было бы желательно детально оценить вероятные отношения так,
чтобы результаты вычислений были как можно более индивидуальными, но
предпринимать полное исследование вероятности отношений в этой работе
было бы не осуществимо. В исследовании такой обширной области как
структура физической вселенной, приходится не только отбирать
раскрываемые темы, но и решать, до какой степени они будут освещаться.
Возможно полезно скрупулезное рассмотрение отношений вероятности,
входящих в физические ситуации, но время и усилие, требующиеся для
выполнения этого проекта, бесспорно, будут огромными, а вклад в основные
цели этого труда недостаточным, чтобы оправдать размещение таких больших
ресурсов. Решения, насколько далеко должно заходить исследование в
конкретных областях, должны приниматься время от времени по ходу работы,
чтобы ограничить ее конечный объем.
В этой связи, хорошо бы указать, что вычисление уникального межатомного
расстояния для каждого элемента или комбинации элементов никогда не
будет возможно, даже когда будут четко установлены отношения
вероятности, поскольку во многих случаях выбор из возможных альтернатив
– это не только вопрос относительной вероятности, но и истории
конкретного образца. Если в области физических условий, при которых
выполняется эмпирическое исследование, устойчивы две или больше
альтернативные формы, обработка, которой уже подвергался образец, играет
важную роль в определении структуры.
Однако из этого не следует, что мы полностью препятствуем получению
определенных величин межатомных расстояний. Хотя еще не существует
количественной оценки относительных вероятностей, природа главных
факторов, включенных в их определение, может быть выведена теоретически.
В большинстве случаев, качественной информации достаточно, чтобы
исключить все, кроме нескольких величин возможных вариаций конкретных
вращений. Кроме того, имеется ряд отношений, посредством которых область
изменчивости может быть сужена еще больше. Эти паттерны станут
очевидными, когда в следующей главе мы будем исследовать расстояния в
соединениях; они будут рассматриваться более детально.
Поскольку мы начинаем анализ факторов, определяющих межатомное
расстояние, первое, что следует подчеркнуть, — мы имеем дело не с
размерами атомов, мы оцениваем расстояние между положениями
равновесия, которые занимают атомы при конкретных условиях. В
главе 1 мы исследовали общую природу атомного равновесия. В этой и
следующей главе мы увидим, как разные факторы, включенные в отношения
между вращениями взаимодействующих атомов, влияют на точку равновесия;
мы придем к величинам межатомных расстояний при статических условиях.
Затем, в главах 5 и 6, мы будем развивать количественные отношения,
которые позволят определить, какие изменения происходят в расстояниях
равновесия, когда вмешиваются внешние силы в виде давления и
температуры.
Как мы видели в предыдущем томе, все атомы и совокупности материи
подвергаются действию двух противоположных сил общей природы: гравитации
и последовательности естественной системы отсчета. Это и есть те
первичные силы (или движения), которые определяют ход физических
событий. Вне гравитационных пределов самых больших совокупностей,
движение наружу за счет последовательности естественной системы отсчета
превышает движение вовнутрь под действием гравитации. Такие
совокупности, главные галактики, удаляются друг от друга со скоростями,
увеличивающимися с расстоянием. Внутри гравитационных пределов,
гравитационное движение больше, и все атомы и молекулы движутся
вовнутрь. В конечном счете, если ничего не вмешивается, движение
вовнутрь несет каждый атом в пределах единицы расстояния другого атома,
и перевороты направления, совершающиеся на границе единицы, приводят к
установлению равновесия между движениями двух атомов. Межатомное
расстояние – это расстояние между центрами атомов в состоянии
равновесия. Это не определение размеров атомов, как считают сейчас.
Современная теория, рассматривающая межатомное расстояние как измерение
“размера”, во многих отношениях схожа с теорией электронной “связи”
молекулярной структуры. Подобно электронной теории, она базируется на
ошибочном допущении. В данном случае, это допущение, что в твердом
состоянии атомы пребывают в контакте. Как и электронная теория, она
годится лишь для относительно небольшого числа веществ в их простой
форме. Поэтому для объяснения отклонений наблюдаемых расстояний от тех,
какими им положено быть, приходится прибегать к изобилию дополнительных
и вспомогательных гипотез. Как говорится в учебниках, даже в металлах,
которые с точки зрения теории являются самыми простыми структурами,
имеется много трудных проблем, включая тот факт, что допускаемый
“размер” меняется в зависимости от кристаллической структуры. Некоторые
дальнейшие аспекты этой ситуации будут рассматриваться в главе 3.
Сходство между этими двумя ошибочными теориями не связано с отсутствием
адекватных основ и природой трудностей, с которыми они сталкиваются.
Оно расширяется до решения этих трудностей, в то время как те же
принципы, выведенные из постулатов Обратной Системы для рассмотрения
образования молекул химических соединений, будучи приложены другим
способом, являются общими рассуждениями, управляющими величиной
внутриатомного расстояния в элементах и соединениях. Бесспорно, все
совокупности электроотрицательных элементов обладают скорее молекулярным
составом, чем атомным, поскольку молекулярное требование — отрицательное
электрическое смещение атома такого элемента должно уравновешиваться
эквивалентным, положительным смещением для достижения устойчивого
равновесия в пространстве — должно применяться и к комбинации с подобным
атомом. Как мы видели при исследовании структурной ситуации,
электроположительные элементы не подвергаются такому ограничению, но во
многих случаях, молекулярный (со сбалансированной ориентацией) вид
структуры превалирует над электроположительной структурой по причине
сопутствующих факторов, влияющих на относительную вероятность.
Вследствие того факта, что расстояния следуют структурному паттерну,
разные способы ориентирования атомных вращений, которые обсуждались в
главе 18 тома 1, с небольшими модификациями за счет конкретных условий,
существующих в совокупностях элементов, определяют способ, как атомы
элемента могут комбинироваться друг с другом и действующие величины
конкретных вращений в этих комбинациях.
На первый взгляд, конкретные вращения электроположительных элементов
основываются на смещениях вращения, описанных в главе 10 тома 1. Там где
межатомная ориентация представляет собой обычную положительную
компоновку, смещения напрямую переводятся в конкретные вращения путем
прибавления первичной единицы, и уменьшения величин приращения там, где
вращение распространяется на вибрацию два. За исключением элементов
группы 2А, которые, как уже отмечалось, являются предметом особых
соображений из-за их низких магнитных смещений, все элементы Деления
I следуют регулярному
электроположительному паттерну конкретных вращений. Единственные
нарушения — электрические вращения вторых и третьих элементов каждой
группы, где точка перехода к вибрации два меняется между группами.
Внутриатомные расстояния в этом делении приводятся в таблице 2.
Регулярный электроположительный паттерн относится и к Делению
II, и ряд элементов группы 3А
Деления II
кристаллизуется на этой основе, с межатомными расстояниями,
определяемыми так же, как и для Деления I.
Однако, как отмечалось в томе 1, элементы Деления
II обычно благоприятствуют
магнитному типу ориентации в химических соединениях, потому что при
увеличении смещения, обычная положительная ориентация становится менее
вероятной. Те же соображения вероятности работают против положительной
ориентации в элементах этого деления, но вместо использования в качестве
альтернативы магнитной ориентации, эти элементы пользуются видом
ориентации, доступным лишь тогда, когда все вращения каждого участника
соединения идентичны друг другу. Такая компоновка переворачивает
действующие направления вращений альтернативных атомов. Итоговое
относительное вращение является комбинацией x
и 8-x (или 4-x),
как при нейтральной ориентации, а действующие конкретные вращения: 10
для вибрации один и 5 для вибрации два. Также обычна величина комбинации
5-10.
Таблица 2: Расстояния — Деление
I
|
Группа |
Атомный |
|
Конкретное вращение |
Расстояние |
||||||||
|
Магнитное |
Электрическое |
Выч. |
Набл. |
|||||||||
|
2B |
11 |
|
3-2½ |
2 |
3,70 |
3,71 |
||||||
|
12 |
|
3-2½ |
2½ |
3,17 |
3,21 |
|||||||
|
13 |
|
3-2½ |
3 |
2,83 |
2,86 |
|||||||
|
3A |
19 |
|
4-3 |
2 |
4,49 |
4,50 |
||||||
|
20 |
|
4-3 |
2½ |
4,00 |
3,98 |
|||||||
|
21 |
|
4-3 |
4 |
3,18 |
3,20 |
|||||||
|
22 |
|
4-3 |
5 |
2,95 |
2,92 |
|||||||
|
3B |
37 |
|
4-4 |
2 |
4,85 |
4,87 |
||||||
|
38 |
|
4-4 |
2½ |
4,32 |
4,28 |
|||||||
|
39 |
|
4-4 |
3½ |
3,64 |
3,63 |
|||||||
|
40 |
|
4-4 |
5 |
3,18 |
3,23 |
|||||||
|
4A |
55 |
|
4½-4½ |
2 |
5,23 |
5,24 |
||||||
|
56 |
|
5-4½ |
3 |
4,36 |
4,34 |
|||||||
|
57 |
|
4½-4½ |
4 |
3,70 |
3,74 |
|||||||
|
58 |
|
5-4½ |
5 |
3,61 |
3,63 |
|||||||
|
4B |
89 |
|
4½-5 |
4 |
3,79 |
3,76* |
||||||
|
90 |
|
|
5 |
|
|
Обратный вид структуры появляется в объемно-центрированных кубических
кристаллических формах хрома и железа, которые сосуществуют с
регулярными положительными шестиугольными или гранецентрированными
структурами. Первые элементы соответствующих групп Деления
II, ванадий и ниобий, сочетают
положительные и обратные ориентации. Выше ниобия, в общих формах
элементов Деления II,
положительная ориентация не появляется, по крайней мере, в тех
структурах, которыми ограничивается нынешнее обсуждение. И все элементы
принимают обратную ориентацию, кроме европия и иттербия, которые
сочетают обратную ориентацию с одним определенным вращением; то есть,
полностью отсутствует электрическое смещение вращения, как у элементов
инертного газа.
На основании соображений, обсужденных в главе 1, среднее действующее
конкретное вращение для таких комбинаций вращения принимается как
геометрическое среднее двух компонентов. Если ориентации одинаковы и
отличаются только по величине, как в комбинации 5-10, и в комбинациях
магнитных вращений, с которыми мы столкнемся позже, равновесие
достигается обычным способом. Если включаются два разных электрических
вращения, двухатомная пара не может достичь пространственного равновесия
индивидуально, но они создают групповое равновесие, аналогичное тому,
которое достигается, когда n
одновалентных атомов каждый комбинируются внутри одного атома
валентности n.
Расстояния Деления II
показаны в Таблице 3.
Таблица 3: Расстояния — Деление
II
|
Группа |
Атомный |
|
Конкретное вращение |
Расстояние |
||||||||
|
Магнитное |
Электрическое |
Выч. |
Набл. |
|||||||||
|
3A |
23 |
|
4-3 |
6-10 |
2,62 |
2,62 |
||||||
|
24 |
|
4-3 |
7 |
2,68 |
2,72 |
|||||||
|
4-3 |
10 |
2,46 |
2,49 |
|||||||||
|
25 |
|
4-3 |
8 |
2,59 |
2,58 |
|||||||
|
26 |
|
4-3 |
8½ |
2,56 |
2,57 |
|||||||
|
4-3 |
10 |
2,46 |
2,48 |
|||||||||
|
27 |
|
4-3 |
9 |
2,52 |
2,51 |
|||||||
|
28 |
|
4-3 |
9½ |
2,49 |
2,49 |
|||||||
|
3B |
41 |
|
4-4 |
6-10 |
2,83 |
2,85 |
||||||
|
42 |
|
4-4½ |
10 |
2,72 |
2,72 |
|||||||
|
43 |
|
4-4½ |
10 |
2,73 |
2,73* |
|||||||
|
44 |
|
4-4½ |
10 |
2,73 |
2,70 |
|||||||
|
45 |
|
4-4 |
10 |
2,66 |
2,69 |
|||||||
|
4-4½ |
10 |
2,73 |
2,76 |
|||||||||
|
46 |
|
4-4½ |
10 |
2,73 |
2,74 |
|||||||
|
4A |
59 |
|
5-4½ |
5 |
3,61 |
3,64 |
||||||
|
60 |
|
5-4½ |
5 |
3,61 |
3,65 |
|||||||
|
62 |
|
5-4½ |
5 |
3,61 |
3,62* |
|||||||
|
63 |
|
4½-5 |
1-5 |
3,96 |
3,96 |
|||||||
|
64 |
|
5-4½ |
5 |
3,61 |
3,62 |
|||||||
|
65 |
|
5-4½ |
5 |
3,61 |
3,59 |
|||||||
|
66 |
|
5-4½ |
5 |
3,61 |
3,58 |
|||||||
|
67 |
|
4½-5 |
5 |
3,52 |
3,56 |
|||||||
|
68 |
|
4½-5 |
5 |
3,52 |
3,53 |
|||||||
|
69 |
|
4½-5 |
5 |
3,52 |
3,52 |
|||||||
|
70 |
|
4½-4½ |
1-5 |
3,86 |
3,87 |
|||||||
|
71 |
|
4½-5 |
5 |
3,52 |
3,50* |
|||||||
|
4B |
91 |
|
4½-5 |
5-10 |
3,22 |
3,24* |
||||||
|
92 |
|
4½4½ |
10 |
2,87 |
2,85 |
|||||||
|
93 |
|
4½-4½ |
5 |
3,43 |
3,46* |
|||||||
|
94 |
|
4½4½ |
5-10 |
3,14 |
3,15* |
|||||||
|
95 |
|
4½-4½ |
5 |
3,43 |
3,46* |
|||||||
|
96 |
|
4½-4½ |
5-10 |
3,14 |
3,10* |
|||||||
|
|
|
|
5 |
|
|
Из-за большей вероятности комбинаций электроположительных видов,
характеристики Деления II
переносятся на первые элементы Деления III,
и эти элементы, никель, палладий и лютеций, включены в таблицу.
Некоторые подобные модификации обычных границ деления уже отмечались в
связи с другими темами.
Общее итоговое вращение материального атома – это вращение с
положительным смещением; то есть, со скоростью меньше единицы. Как
таковое, такое смещение обычно приводит к изменению положения в
пространстве. Однако внутри единицы пространства, все движение является
движением во времени. Следовательно, ориентация атома с целью
пространственно-временного равновесия существует в трех измерениях
времени. Как мы видели в исследовании межрегиональной ситуации в главе
12 тома 1, каждое из измерений индивидуально контактирует с
пространством региона вне единицы расстояния. В той степени, в которой
движение в измерении времени действует вдоль линии контакта, оно
является движением в эквивалентном пространстве. В противном случае, оно
не обладает пространственным действием выше границы единицы. Из-за
независимости трех измерений движения во времени, относительная
ориентация электрического вращения любой комбинации атомов может быть
одинаковой со всеми измерениями пространства или могут быть две или три
разных ориентации.
У большинства уже обсужденных элементов, ориентация одинакова во всех
измерениях пространства, а в исключениях альтернативные вращения
симметрично распределяются в твердой структуре. Система сил
совокупности таких элементов однородна. Из этого следует, что любая
совокупность атомов этих элементов обладает структурой, в которой
составляющие организованы в одном из геометрических паттернов, возможных
для равных сил: равновеликий кристалл. Все электроположительные элементы
(Деления I и
II) кристаллизуются в
равновеликих формах, и за исключением некоторых, обладающих более
сложными структурами, каждая кристаллическая форма этих элементов
принадлежит одному или другому их трех типов: объемно-центрированной,
кубической гранецентрированной или шестиугольной плотноупакованной
структуры.
Сейчас мы переходим к другому главному подразделению элементов,
электроотрицательному классу, элементам, чье нормальное электрическое
смещение отрицательное. Здесь, система сил не обязательно однородна,
поскольку самая вероятная компоновка в одном или двух измерениях может
быть отрицательной ориентацией, прямой комбинацией двух отрицательных
электрических смещений, аналогичной обще-положительным комбинациям.
Нельзя иметь отрицательную ориентацию во всех трех измерениях. И если
она существует в одном или двух измерениях, силы вращения атомов
обязательно неоднородны. Контролирующий фактор – требование, чтобы общее
итоговое смещение вращения материального атома как целого было
положительным. Очевидно, что отрицательная ориентация во всех трех
измерениях несовместима с этим требованием. Но если отрицательное
смещение ограничивается одним измерением, совокупность обладает
фиксированными атомными положениями в двух измерениях, с фиксированным
средним положением в третьем измерении из-за положительного смещения
атома в целом. Это приводит к кристаллической структуре, которая, по
сути, эквивалентна одному из фиксированных положений во всех измерениях.
Обычно, такие кристаллы не изомерны, поскольку межатомное расстояние в
четном измерении обычно отличается от межатомного расстояния двух
других. Если случится так, что расстояния во всех измерениях совпадают,
в последующем обсуждении мы обнаружим, что симметрия пространства не
является указателем на симметрию сил.
Если отрицательное смещение совсем невелико, как у нижних элементов
Деления IV,
отрицательную ориентацию в двух измерениях можно иметь, если
положительное смещение в третьем измерении превышает сумму двух
отрицательных компонентов так, что итоговый результат все еще
положительный. Здесь, относительные положения атомов фиксируются лишь в
одном измерении, но средние положения в двух других измерениях постоянны
по причине итогового, положительного смещения атомов. Совокупность таких
атомов сохраняет большинство внешних характеристик кристалла, но при
исследовании внутренней структуры, представляется, что атомы
распределяются скорее случайно, чем в обычной упорядоченной компоновке
кристалла. На самом деле, здесь имеется столько же порядка, сколько и в
кристаллической структуре, но часть порядка пребывает скорее во времени,
чем в пространстве. Такая форма материи определяется как стекловидная
или стеклообразная форма, в отличие от кристаллической формы.
В этой связи, термин “состояние” часто употребляется вместо “формы”, но
физическое состояние материи обладает и другим значением, основанном на
других критериях. Поэтому, представляется целесообразным свести
использование этого термина к одному применению. И стекла, и кристаллы
пребывают в твердом состоянии.
Приступая к рассмотрению структур отдельных электроотрицательных
элементов, мы будем начинать с Деления III.
Общая ситуация в этом делении аналогична ситуации в Делении
II, но отрицательность
обычного электрического смещения вносит новый фактор в определение
паттерна ориентации, поскольку самая вероятная ориентация
электроотрицательного элемента может не существовать во всех трех
измерениях. Как констатировалось раньше, если в данном наборе
обстоятельств возможны две или более разных ориентаций, решающим
фактором является относительная вероятность. Низкие смещения более
вероятны, чем высокие. Простые ориентации более вероятны, чем
комбинации. Положительная электрическая ориентация более вероятна, чем
отрицательная. В Делении I,
все эти факторы работают в одинаковом направлении. Положительная
ориентация проста и обладает наименьшей величиной смещения.
Следовательно, все структуры этого деления формируются на основе
положительной ориентации. В Делении II,
поле вероятности уже. Здесь, положительное смещение
x больше, чем обратное
смещение 8-x, и это
работает против большей неотъемлемой вероятности простой положительной
структуры. В результате, в этом делении обнаруживаются и положительные и
отрицательные виды структур, наряду с комбинацией обоих.
В Делении III,
отрицательная ориентация обладает статусом, похожим на статус
положительной ориентации в делении II.
Как простая ориентация, она обладает относительно большей вероятностью.
Но она ограничена одним измерением. Следовательно, структуры Групп 3А и
3В Деления III
неоднородны, с обратной ориентацией в двух других измерениях. Возможно
сочетание двух видов ориентации. У меди и серебра, первых элементов
соответствующих групп Деления III,
кристаллы формируются на основе комбинированной ориентации, обладающей
кубической симметрией. Как и в Делении II,
элементы Групп 4А и 4В Деления III,
кристаллизуются полностью на основе обратной ориентации. Таблица 4
приводит то, что может рассматриваться как правильные межатомные
расстояния элементов Деления III.
Таблица 4: Расстояния — Деление III
|
Группа |
Атомный |
Элемент |
Удельное |
Расстояние |
||||||||
|
Магнитное |
Электрическое |
Выч. |
Набл. |
|||||||||
|
3A |
29 |
Медь |
4-3 |
8-10 |
2,53 |
2,55 |
||||||
|
30 |
Цинк |
4-4 |
7 |
2,90 |
2,91 |
|||||||
|
4-4 |
10 |
2,66 |
2,66 |
|||||||||
|
31 |
Галлий |
4-3 |
6 |
2,79 |
2,80 |
|||||||
|
4-3 |
10 |
2,46 |
2,44 |
|||||||||
|
3B |
47 |
Серебро |
4-5 |
8-10 |
2,87 |
2,88 |
||||||
|
48 |
Кадмий |
5-4 |
7 |
3,20 |
3,26* |
|||||||
|
5-4 |
10 |
2,94 |
2,97 |
|||||||||
|
49 |
Индий |
5-4 |
6 |
3,33 |
3,37 |
|||||||
|
5-4 |
6-10 |
3,21 |
3,24 |
|||||||||
|
4A |
72 |
Гафний |
4-4½ |
5 |
3,26 |
3,32 |
||||||
|
73 |
Тантал |
4½-4½ |
10 |
2,87 |
2,86 |
|||||||
|
74 |
Вольфрам |
4-4½ |
10 |
2,73 |
2,74 |
|||||||
|
75 |
Рений |
4-4½ |
10 |
2,73 |
2,77* |
|||||||
|
76 |
Осмий |
4-4½ |
10 |
2,73 |
2,73 |
|||||||
|
77 |
Иридий |
4-4½ |
10 |
2,73 |
2,71 |
|||||||
|
78 |
Платина |
4-4½ |
10 |
2,73 |
2,77 |
|||||||
|
79 |
Золото |
4½-4½ |
10 |
2,87 |
2,88 |
|||||||
|
80 |
Меркурий |
4-4½ |
5-10 |
2,98 |
3,00 |
|||||||
|
4½-4½ |
5 |
3,43 |
3,47 |
|||||||||
|
81 |
Таллий |
4½-4½ |
5 |
3,43 |
3,45 |
Хотя в Делении IV
вероятность отрицательной ориентации больше, чем в Делении
III, за счет меньших величин
смещения, этот вид структуры редко появляется в кристаллах низкого
деления. Причина в следующем: Если у элементов с низким смещением
существует такая ориентация, она существует в двух измерениях, и создает
скорее стекловидную или стеклообразную совокупность, чем кристалл.
Обратная ориентация не подвергается никакому ограничивающему фактору
такой природы, но она менее вероятна при низких смещениях. За
исключением группы 4А, где она продолжает доминировать, такая ориентация
менее часта по мере уменьшения смещения. Там же, где она существует, она
все больше и больше комбинируется с другим видом ориентации. В
результате этих ограничений, применимых к более вероятным видам
ориентации, многие структуры деления IV
формируются на основе вторичной, положительной ориентации, комбинации
двух смещений 8 — x.
В электроположительных делениях, вторичная,
положительная ориентация не возможна, поскольку в этих делениях 8 —
x отрицательная, и
подобно самой отрицательной ориентации, отрицательная комбинация 8 —
x должна принимать
подчиненную роль в одном или двух измерениях асимметричной структуры.
Такая кристаллическая структура не может соперничать с высокой
вероятностью симметричных электроположительных кристаллов и,
следовательно, не существует. Однако в электроотрицательных делениях,
смещение 8 – x
положительное, и здесь нет ограничений, кроме тех, которые возникают за
счет высоких величин смещения.
Действующее смещение вторичной, положительной ориентации
даже больше, чем можно было бы ожидать от величины количества 8 –
x, поскольку изменение нулевых
точек для двух противоположно направленных движений тоже направлено
противоположно, и новые нулевые точки находятся на расстоянии 16–ти
единиц смещения друг от друга. Итоговое результирующее смещение равно 16
– 2x, и соответствующее
удельное вращение 18 – 2x.
В Делении IV, числовые
величины последнего выражения лежат в области от 10 до 16. За счет
низкой вероятности таких высоких вращений, вторичная, положительная
ориентация ограничена одним или половиной измерения, несмотря на ее
положительный характер. В Делении III,
смещения 8 – x ниже, но
в этом случае они слишком низкие. Двух единичное разделение нулевых
точек (16 единиц смещения) не может поддерживаться до тех пор, пока
действующее смещение не станет равно, по крайней мере, 8-ми (одной
полной трехмерной единице). Поэтому, вторичная, положительная ориентация
ограничена делением IV.
Особый вид структуры возможен лишь у тех элементов,
которые обладают смещением вращения в четыре единицы в электрическом
измерении. Эти элементы находятся на границе между Делениями
III и
IV, где одинаково вероятны
вторичные, положительные и обратные ориентации. При таких условиях,
другие элементы кристаллизуются в шестиугольные или четырехугольные
структуры, использующие разные ориентации в разных измерениях. Однако у
4-х элементов с такими смещениями, две ориентации создают одинаковое
удельное вращение: 10. Следовательно, межатомное расстояние в этих
кристаллах одинаково во всех измерениях, и кристаллы однородны, хотя
силы вращения в разных измерениях не носят одинакового характера.
Молекулярная компоновка в этом кристаллическом паттерне, ромбовидная
структура, демонстрирует истинную природу сил вращения. Внешне этот
кристалл нельзя отличить от однородных кубических кристаллов, но
аналогичная объемноцентрированная структура имеет атом в каждом углу
куба и один в центре куба, в то время как ромбовидная структура
оставляет противолежащие углы открытыми для приспособления к необычной
проекции сил во вторичном, положительном измерении.
У низких элементов Деления IV,
пребывающиих выше области обратного вида ориентации, нет доступной
альтернативы для комбинации с вторичной, положительной ориентацией.
Поэтому, кристаллы этих элементов не обладают действующим электрическим
вращением в оставшихся измерениях. Относительное удельное вращение в
этих измерениях равно единице, как и у всех элементов инертного газа.
Наиболее общие расстояния у совокупностей элементов Деления
IV показаны в Таблице 5.
Таблица 5: Расстояния — Деление IV
|
Группа |
Атомный |
|
Удельное вращение |
Расстояние |
||||||||
|
Магнитное |
Электрическое |
Выч. |
Набл. |
|||||||||
|
2B |
14 |
|
3-3 |
5-10 |
2,31 |
2,35 |
||||||
|
15 |
|
3-3 |
10 |
2,19 |
2,2 |
|||||||
|
3-4 |
||||||||||||
|
3-4 |
1 |
3,46 |
3,48* |
|||||||||
|
16 |
|
3-3 |
10 |
2,11 |
2,07 |
|||||||
|
3-3 |
1 |
3,21 |
3,27* |
|||||||||
|
17 |
|
3-3 |
16 |
1,92 |
1,82 |
|||||||
|
3-3 |
1-16 |
2,48 |
2,52 |
|||||||||
|
3A |
32 |
|
4-3 |
10 |
2,46 |
2,43 |
||||||
|
33 |
|
4-3 |
12 |
2,37 |
2,44* |
|||||||
|
4-3 |
10 |
2,46 |
2,51 |
|||||||||
|
34 |
|
4-3 |
14 |
2,32 |
2,32 |
|||||||
|
3-4 |
1 |
3,46 |
3,46 |
|||||||||
|
35 |
|
4-3 |
16 |
2,25 |
2,27 |
|||||||
|
3-4 |
1 |
3,46 |
3,30 |
|||||||||
|
3B |
50 |
|
4½-4 |
10 |
2,80 |
2,80 |
||||||
|
5-4 |
5-10 |
3,22 |
3,17 |
|||||||||
|
5-4 |
10 |
2,94 |
3,02 |
|||||||||
|
51 |
|
5-4 |
12 |
2,83 |
2,87 |
|||||||
|
5-4 |
4-10 |
3,34 |
3,36* |
|||||||||
|
52 |
|
5-4½ |
14 |
2,82 |
2,86 |
|||||||
|
5-4½ |
1-10 |
3,71 |
3,74 |
|||||||||
|
53 |
|
5-4 |
16 |
2,68 |
2,70 |
|||||||
|
5-4 |
1-16 |
3,54 |
3,54 |
|||||||||
|
5-4 |
1 |
4,46 |
4,41* |
|||||||||
|
4A |
82 |
|
4½-4½ |
5 |
3,43 |
3,49 |
||||||
|
83 |
|
4½-4½ |
5 |
3,43 |
3,47* |
|||||||
|
4½-4½ |
5-10 |
3,14 |
3,10 |
|||||||||
|
84 |
|
|
5 |
|
|
Вплоть до этого момента, не уделялось никакого внимания
элементам с атомным номером ниже 10, поскольку силы вращения этих
элементов подвергаются определенным конкретным влияниям, что делает
желательным их отдельное обсуждение. Одна причина отклонения от
нормального поведения – маленький размер вращающихся групп. В больших
группах различаются четыре измерения, и за исключением некоторых
перекрываний, каждое измерение обладает своими характерными комбинациями
сил, что мы видели в предыдущих параграфах. Однако в группе из 8-ми
элементов, вторые серии четырех элементов, которые обычно составляли бы
деление III, на самом
деле находятся в положении Деления IV.
В результате, до некоторой степени, эти четыре элемента обладают
свойствами обоих делений. Аналогично, элементы этих групп Деления
I могут работать, как будто бы
они являются членами Деления III.
Вторичное влияние, действующее на силы и кристаллические структуры
элементов низких групп, — бездействие сил вращения в конкретных
измерениях, упомянутых раньше.
Удельное вращение двух единиц не действует в
положительном направлении. Причина этого раскрывается в уравнении 1 – 1.
Применяя это уравнение, мы находим, что действующая сила вращения (ln
t) для t
= 2 составляет 0,693, что меньше, чем противоположная
пространственно-временная сила, равная 1. Следовательно, итоговая
действующая сила удельного вращения, равная 2, ниже минимальной величины
для действия в положительном направлении. Чтобы создавать действующую
силу, удельное вращение должно быть достаточно высоким, чтобы сделать
ln t больше единицы.
Это достигается во вращении 3.
Удельное магнитное вращение группы 1В, включающее лишь
два элемента, водород и гелий, и 8 элементов группы 2А, начиная с лития,
сочетает величины 3 и 2. Если величина 2 применяется к вспомогательному
вращению (3-2), одно измерение не активно; если она применяется к
основному вращению (2-3), не активны два измерения. Это уменьшает силу,
оказываемую каждым атомом, до 2/3 нормальной величины в случае одного
неактивного измерения и до 1/3 для двух не активных измерений.
Межатомное расстояние пропорционально квадратному корню произведения
двух вовлеченных сил. Следовательно, уменьшение в расстоянии тоже равно
1/3 на каждое не активное измерение.
Поскольку электрическое вращение не является базовым
движением, а обратным вращением магнитно-вращающейся системы,
ограничения, которым подвергается базовое вращение, не работают.
Электрическое вращение просто изменяет магнитное вращение, и низкая
величина силы, свойственная удельному вращению 2, проявляется как
межатомное расстояние, большее чем то, которое превалировало бы, если бы
электрического смещения вообще не было (единицы удельного вращения).
Теоретические величины межатомных расстояний элементов
низких групп сравниваются с измеренными величинами в Таблице 6.
Цифры в скобках в колонке 4 этой таблицы указывают на
действующее число измерений. Таким образом, обозначение 3(1), показанное
для водорода, означает, что этот элемент обладает удельным магнитным
вращением 3, действующим лишь в одном измерении.
За исключением того, когда кристаллы равновелики, в
связи с измерениями расстояния элементов нижних групп имеется много
неопределенности. Зафиксированные многие другие дополнительные величины
тоже включены в таблицу. Эта ситуация будет подробнее обсуждаться в
главе 3, где мы воспользуемся измерениями расстояний между похожими
атомами, которые являются составляющими химических соединений.
Таблица 6: Расстояния – Элементы нижней группы
|
Группа |
Атомный |
|
Удельное |
Расстояние |
||||||||
|
Магнитное |
Электрическое |
Выч. |
Набл. |
|||||||||
|
1B |
1 |
Водород |
3(1) |
10 |
0,70 |
0,74* |
||||||
|
2 |
Гелий |
3(1) |
1 |
1,07 |
1,09 |
|||||||
|
*2A |
3 |
Литий |
2½-2½ |
2 |
3,05 |
3,03 |
||||||
|
4 |
Бериллий |
3(2) |
2½ |
2,282 |
2,28 |
|||||||
|
5 |
Бор |
3(2) |
5 |
1,68 |
1,74* |
|||||||
|
3-3 |
10 |
2,11 |
2,03* |
|||||||||
|
6 |
Углерод |
3(2) |
5-10 |
1,54 |
1,54 |
|||||||
|
Углерод |
3(2) |
1 |
1,41 |
1,42 |
||||||||
|
3-3 |
1 |
3,21 |
3,40 |
|||||||||
|
7 |
Азот |
3(1½) |
10 |
1,06 |
1,06 |
|||||||
|
3-3 |
1 |
3,21 |
3,44* |
|||||||||
|
8 |
Кислород |
3(1½) |
10 |
1,06 |
1,15* |
|||||||
|
3-3 |
1 |
3,21 |
3,20* |
|||||||||
|
9 |
Фтор |
3(2) |
||||||||||
|
10 |
1,41 |
1,44* |
Как указывалось во вводных параграфах этой главы, мы еще
не в том положении, когда можем определять, каким будет межатомное
расстояние для любого данного элемента при данном наборе условий.
Обсужденные теоретические соображения во многих случаях реально дают
конкретные величины, но в других примерах имеется неопределенность,
поскольку наблюдаемой структуре соответствуют две или больше
теоретически возможных компоновок смещения. И в теоретической, и в
экспериментальной области происходит непрерывный прогресс, и можно
ожидать, что неопределенности постепенно сведутся к минимуму,
упомянутому раньше. В ходе процесса, обязательно произойдут изменения в
отождествлениях наблюдаемых расстояний с теоретически возможными
структурами. Сравнение таблиц 1-6 с соответствующими таблицами первого
издания было бы интересно как указание на природу и величину изменений,
которые произошли в нашей точке зрения на ситуацию с межатомным
расстоянием за последние двадцать лет, и, посредством расширения, как
указание на объем изменения, которое можно ожидать в будущем.
Такое сравнение показывает, что модификации начальных
выводов, которые требуются сейчас, в свете доступной дополнительной
информации, почти полностью совпадают с теми, которые возникли в
результате лучшего теоретического понимания поведения удельных магнитных
вращений выше действующей величины 4. Несколько изменений требуется либо
в магнитных, либо в электрических величинах в тех комбинациях вращения,
в которых удельное магнитное вращение равно 4-4 или меньше.
Одной из сбивающих с толку ситуаций вращения, как это
представлялось во время первой публикации, была кажущаяся обратной
последовательность удельного магнитного вращения в Группах 4А и 4В. В то
время считалось, что величины 4½ и 5 удельного вращения соответствуют
одинаковому смещению 4, с той лишь разницей, что в случае величины 4½
вращение распространяется на две единицы вибрации, а последнее
приращение удельного вращения в этом случае равно только половине
размера. Следующее приращение на половину единицы, если бы оно было
возможно, привело бы вращение 4½ назад, к величине 5. Таким образом,
представлялось, что последовательность удельных вращений выше 4½-4 была
бы 4½-4½, 5-4½, 5-5, и так далее. Но тенденция идет в противоположном
направлении. По мере увеличения атомного номера, вместо движения к более
высоким величинам происходит движение к меньшим величинам. Это было
очевидно уже во время публикации первого издания, поскольку меньшие
межатомные расстояния ряда элементов от вольфрама до платины не могли
приниматься в расчет до тех пор, пока магнитное удельное вращение не
падало назад к 4-4½ с более высоких уровней предшествующих элементов
Группы 4А. Тенденция уменьшения оказалась еще важнее, когда стали
доступны расстояния для дополнительных элементов Группы 4В, поскольку
некоторые из величин указывали на удельные магнитные вращения 4–4 или
даже 4-3½.
Случилось так, что продолжение тенденции к низким величинам в более
поздних данных повлияло на прояснение ситуации. Сейчас очевидно, что в
доступной части Групп 4А и 4В удельное вращение 5–5 не достигается.
(Рассмотрения, которые будут обсуждаться позже, показывают, что удельное
вращение 5-5 было бы нестабильным.) Низкие величины в Группах 4А и 4В
возникают не в результате уменьшения магнитного смещения, а за счет
сдвига существующих единиц смещения с вибрации один к вибрации два,
процесс, который наполовину уменьшает удельное вращение единиц. На
основе вибрации один, смещения вращения 4-3 соответствует удельным
вращениям 5-4. Переход последующих единиц смещения к вибрации два, без
изменения числа единиц смещения, выливается в ряды удельных вращений
5-4, 4½-4, 4-4½, 4-4, и так далее. Подобные серии с одной дополнительной
единицей смещения проходят через величины 5-4½, 4½-5, 4½-4½, 4½-4, и так
далее, а затем следуют тому же пути, что и серии с более низким
смещением.
Модификации, сделанные в теоретических величинах вращения, относятся к
элементам двух групп с самым высоким вращением, поскольку публикация
первого издания является результатом рассмотрения ситуации в свете
нового понимания тенденции удельного вращения. Общий паттерн в Группе 4А
сейчас видится как серии от 5-4½ до 4-4½, с возвращением к 4½-4½ у
низких электроотрицательных элементов. Насколько определено сейчас,
Группа 4В следует тому же паттерну, но продвинутому на один шаг, то есть
она начинается с 4½-5, а не с 5-4½.
Разница в межатомном расстоянии, соответствующая одному из шагов в
процессе перехода, относительно мала. И в свете значительной вариации в
экспериментальных величинах представлялось целесообразным принять во
внимание вероятность комбинаций, таких как удельное вращение 4½-5 одного
из пары атомов и 4½-4½ другого. Ясно, что такие комбинации существуют у
некоторых элементов низких групп, например, у натрия, и, возможно,
играют определенную роль в более высоких группах. Например, большинство
зафиксированных расстояний у гольмия и эрбия лучше согласуются с
комбинацией 5-4½ и 4½-5, чем с какой-либо из них по отдельности. Однако
теоретически возможны все приведенные величины, и единственная проблема
в этом и в других подобных случаях, какая теоретическая величина
соответствует наблюдаемому расстоянию. Ответам на этот вопрос придется
подождать оценки теоретических вероятностей или разрешения
экспериментальных неясностей.
Многим вопросам, касающимся структур альтернативных кристаллов, тоже
придется подождать большей информации из теории или эксперимента,
особенно если рассматриваются кристаллические формы, существующие лишь
при высоких температурах или давлениях. Однако в этой области уже
имеется большой объем информации. Ее можно связать с теоретической
картиной, как только у кого-то появится время и желание выполнить эту
задачу.
From Wikipedia, the free encyclopedia
(Top) Diamond crystal structure, depicting an atomic spacing of 0.154 nm. (Bottom) Graphite crystal structure, depicting an atomic spacing of 0.142 nm.
Atomic spacing refers to the distance between the nuclei of atoms in a material. This space is extremely large compared to the size of the atomic nucleus, and is related to the chemical bonds which bind atoms together.[1] In solid materials, the atomic spacing is described by the bond lengths of its atoms. In ordered solids, the atomic spacing between two bonded atoms is generally around a few ångströms (Å), which is on the order of 10−10 meters. However, in very low density gases (for example, in outer space) the average distance between atoms can be as large as a meter. In this case, the atomic spacing isn’t referring to bond length.
The atomic spacing of crystalline structures is usually determined by passing an electromagnetic wave of known frequency through the material, and using the laws of diffraction to determine its atomic spacing. The atomic spacing of amorphous materials (such as glass) varies substantially between different pairs of atoms, therefore diffraction cannot be used to accurately determine atomic spacing. In this case, the average bond length is a common way of expressing the distance between its atoms.
Example[edit]
Bond length can be determined between different elements in molecules by using the atomic radii of the atoms. Carbon bonds with itself to form two covalent network solids.[2] Diamond’s C-C bond has a distance of Sqrt[3]a/4 ≈ 0.154 nm away from each carbon since adiamond ≈ 0.357 nm, while graphite’s C-C bond has a distance of a/Sqrt[3] ≈ 0.142 nm away from each carbon since agraphite ≈ 0.246 nm. Although both bonds are between the same pair of elements they can have different bond lengths.[3]
References[edit]
- ^ Kittel, Charles (2004-11-11). Introduction to Solid State Physics (8th ed.). Wiley. ISBN 047141526X.
- ^ Rossi, Miriam. «How can graphite and diamond be so different if they are both composed of pure carbon?». Scientific American. Scientific American. Retrieved October 9, 2007.
- ^ Brown; Lemay; Bursten (1997). Chemistry the Central Science. Upper Saddle River, NJ: Simon and Schuster. pp. 412–413.
Чтобы разобраться в вопросе, что в современной науке называется радиусом атома, вспомним, что из себя представляет сам атом. По классическим представлениям в центре атома находится ядро, состоящее из протонов и нейтронов, а вокруг ядра каждый на своей орбите вращаются электроны.
Содержание:
- Радиус атома в физике
- Атомный радиус в химии и кристаллографии
- Какие бывают виды
- Как зависит от типа химической связи
- Видео
Радиус атома в физике
Поскольку в данной модели строения атома электроны являются пространственно ограниченными частицами, т. е. корпускулами, логично считать атомным радиусом (а. р.) расстояние от его ядра до самой дальней, или внешней, орбиты, по которой вращаются так называемые валентные электроны.
Однако по современным, квантовомеханическим представлениям, определить данный параметр нельзя так однозначно, как это делается в классической модели. Здесь электроны уже не представляются в виде частиц-корпускул, а получают свойства волн, т. е. пространственно-неограниченных объектов. В такой модели точно определить положение электрона просто невозможно. Здесь эта частица уже представляется в виде электронной орбитали, плотность которой меняется, в зависимости от расстояния до ядра атома.
Итак, в современной модели строения атома его радиус нельзя определить однозначно. Поэтому в квантовой физике, общей химии, физике твердого тела и других смежных науках эту величину сегодня определяют как радиус сферы, в центре которой находится ядро, внутри которой сосредоточено 90-98% плотности электронного облака. Фактически это расстояние и определяет границы атома.
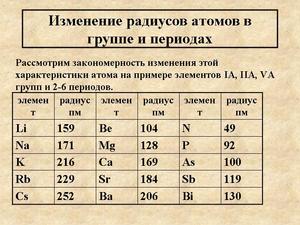
Если рассмотреть Периодическую таблицу химических элементов (таблицу Менделеева), в которой приведены атомные радиусы, можно увидеть определенные закономерности, которые выражаются в том, что в пределах периода эти числа уменьшаются слева направо, а в пределах группы они увеличиваются сверху вниз. Такие закономерности объясняются тем, что внутри периода при движении слева направо заряд атома возрастает, что увеличивает силу притяжения им электронов, а при движении внутри группы сверху вниз все больше заполняется электронных оболочек.
Атомный радиус в химии и кристаллографии
Какие бывают виды
Данная характеристика сильно варьируется, в зависимости от того, в какой химической связи состоит атом. Поскольку все вещества в природе в подавляющем своем большинстве состоят из молекул, понятие а. р. используют для определения межатомных расстояний в молекуле. А данная характеристика зависит от свойств входящих в молекулу атомов, т. е. их положения в Периодической системе химических элементов. Обладая разными физическими и химическими свойствами, молекулы образуют все огромное разнообразие веществ.
По сути, эта величина очерчивает сферу действия силы электрического притяжения ядра атома и его внешних электронных оболочек. За пределами этой сферы в действие вступает сила электрического притяжения соседнего атома. Существует несколько типов химической связи атомов в молекуле:
- ковалентная;
- ионная;
- металлическая;
- ван-дер-ваальсова.
Соответственно этим связям таким же будет и атомный радиус.
Как зависит от типа химической связи
При ковалентной связи АР определяется как половина расстояния между соседними атомами в одинарной химической связи Х—Х, причем Х — это неметалл, ибо данная связь свойственна неметаллам. Например, для галогенов ковалентный радиус будет равен половине межъядерного расстояния Х—Х в молекуле Х2, для молекул селена Se и серы S — половине расстояния Х—Х в молекуле Х8, для углерода С он будет равен половине кратчайшего расстояния С—С в кристалле алмаза.
Данная химическая связь обладает свойством аддитивности, т. е. суммирования, что позволяет определять межъядерные расстояния в многоатомных молекулах. Если связь в молекуле двойная или тройная, то ковалентный АР уменьшается, т. к. длины кратных связей меньше одинарных.
При ионной связи, образующейся в ионных кристаллах, используют значения ионного АР для определения расстояния между ближайшими анионом и катионом, находящимися в узлах кристаллической решетки. Такое расстояние определяется как сумма радиусов этих ионов.
Существует несколько способов определения ионных радиусов, при которых отличаются значения у индивидуальных ионов. Но в результате эти способы дают примерно одинаковые значения межъядерных расстояний. Эти способы или системы были названы в честь ученых, проводивших в этой области соответствующие исследования:
- Гольдшмидта;
- Полинга;
- Белова и Бокия;
- других ученых.
При металлической связи, возникающей в кристаллах металлов, АР принимаются равными половине кратчайшего расстояния между ними. Металлический радиус зависит от координационного числа К. При К=12 его значение условно принимается за единицу. Для координационных чисел 4, 6 и 8 металлические радиусы одного и того же элемента соответственно будут равны 0.88, 0.96 и 0.98.
Если взять два разных металла и сравнить металлические радиусы их элементов, то близость этих значений друг к другу будет означать необходимое, но недостаточное условие взаимной растворимости этих металлов по типу замещения. Например, жидкие калий К и литий Li в обычных условиях не смешиваются и образуют два жидких слоя, потому что их металлические радиусы сильно различаются (0.236 нм и 0.155 нм соответственно), а калий К с цезием Cs образуют твердый раствор благодаря близости их радиусов (0.236 нм и 0.268 нм).
Ван-дер-ваальсовы АР используют для определения эффективных размеров атомов благородных газов, а также расстояний между ближайшими одноименными атомами, принадлежащими разным молекулам и не связанными химической связью (пример — молекулярные кристаллы). Если такие атомы сблизятся на расстояние, меньшее суммы их ван-дер-ваальсовых радиусов, между ними возникнет сильное межатомное отталкивание. Эти радиусы определяют минимально допустимые границы контакта двух атомов, принадлежащих соседним молекулам.
Кроме того, данные АР используют для определения формы молекул, их конформаций и упаковки в молекулярных кристаллах. Известен принцип «плотной упаковки», когда молекулы, образующие кристалл, входят друг в друга своими «выступами» и «впадинами». На основе этого принципа интерпретируются данные кристаллографии и предсказываются структуры молекулярных кристаллов.
Видео
Это полезное видео поможет вам понять, что такое радиус атома.
Металлы — железо, кобальт, никель, гадолиний, диспрозий и некоторые из их сплавов и соединений являются ферромагнитными при температуре ниже критической для каждого соединения. Причина ферромагнетизма до объяснения ее квантовой механикой была неизвестна. Вопрос заключается в том, почему электроны на неполностью заполненных оболочках выстраиваются в направлении приложенного поля и почему они сохраняют эту ориентацию даже после снятия магнитного поля Объясняется это тем, что низшим энергетическим состоянием для некоторых твердых тел является состояние, в котором спины электронов параллельны, а не антипараллельны, как, например, для двух электронов в молекуле водорода. Ферромагнетизм возможен только при определенных межатомных расстояниях и определенных радиусах -орбиталей, поэтому он наблюдается лишь для некоторых элементов. Ферромагнитные вещества проявляют гистерезис в магнитных свойствах. Это означает, что магнитный момент зависит от магнитной предыстории образца кривые зависимости магнитного момента от напряженности магнитного поля различны для случаев, когда магнитное поле увеличивается или уменьшается. [c.497]
Определение межатомного расстояния С—N по вращательно-колебательно электронному спектру [c.70]
Определение межатомного расстояния и частоты основной полосы поглощения H I по вращательно-колебательному спектру поглощения [c.61]
Необходимо раскрыть содержание термина энергия связи . Схема потенциальной энергии произвольной А—В-связи в многоатомной молекуле (рис. 4.1) служит для объяснения данного понятия. Для многоэлектронных атомов, как было отмечено выше, следует учитывать, что валентное состояние может лежать выше соответствующего основного состояния. Если в таком случае два атома находятся в своих основных состояниях, то никакой связи между ними возникнуть не может если же они сближаются друг с другом, то их потенциальная энергия будет возрастать. На определенном межатомном расстоянии потенциальная энергия системы будет приближаться к энергии атомов в валентных состояниях (рис. 4.1, пунктирная линия), и может произойти переход к связанному состоянию. Поэтому внутренняя энергия связи Е равна разности энергий основного молекулярного состояния и валентного состояния, соответствующего бесконечному расстоянию между атомами. Энергия диссоциации О меньше Е на величину энергии нулевых колебаний /lv/2 н на сумму Р энергий перехода, гибридизации, полярного и стерического упорядочения, необходимых для достижения валентного состояния. Разность между энергией нулевых колебаний и максимумом кривой потенциальной энергии равна [c.100]
Методы определения межатомных расстояний в кристаллах рассмотрены на стр. 249—253. [c.80]
Наиболее четкая дифракционная картина, получаемая при максимальном упорядочивании (для монокристаллов), приводит к полной расшифровке структуры с определением межатомных расстояний внутри молекулы и между атомами соседних молекул, углов между связями, геометрии элементарной ячейки, распределения электронной плотности. При исследовании поликристаллов применяют фазовый рентгеноструктурный анализ, который ограничивается получением характерных дифрактограмм и определением меж-плоскостных расстояний для обнаружения и идентификации соединений. [c.200]
Инфракрасная (ИК) спектроскопия используется в различных областях науки, и в каждой из них придается- этому термину различный смысл. Для химика-аналитика это удобный метод решения таких задач, как, например, определение пяти изомеров гексахлорциклогексана, качества парафина, смолы, полимера, эмульгатора в эмульсии для полировки, опознание страны, из которой вывезен контрабандный опиум. Физику ИК-спектроскопия представляется методом исследования энергетических уровней в полупроводниках или определения межатомных расстояний в молекулах. Она может быть также полезна и при измерении температуры пламени ракетного двигателя. Для химика-органика это метод идентификации органических соединений, позволяющий выявлять функциональные группы в молекулах и следить за ходом химических реакций. Для биолога ИК-спектроскопия — перспективный метод изучения транспорта биологически активных веществ в живой ткани, ключ к структуре многих естественных антибиотиков и путь познания строения клетки. Физикохимику метод позволяет приблизиться к пониманию механизма гетерогенного катализа и кинетики сложных реакций. Он служит дополнительным источником информации при расшифровке структуры кристаллов. В этих и многих других областях знания ИК-спектроскопия служит исследователям мощным средством изучения тайн вещества. Вероятно, справедливо будет сказать, что из всех инструментальных методов ИК-спектроскопия наиболее универсальна. [c.9]
Если молекула содержит более двух атомов, то экспериментальная кривая интенсивности определится суммой кривых, описываемых уравнением (2.57). При этом положение первого максимума может не соответствовать значению 7 1. В этом случае для определения межатомных расстояний применяют методы, описанные в гл. 5. Для жидкостей и аморфных тел вычисление среднего значения двойной суммы в выражении (2.54) производят посредством радиальной функции распределения [c.43]
Дублетными, триплетными и секстетными реакциями и иногда их последовательностью практически с исчерпывающей полнотой охватывается все богатство известных гетерогенно-каталитических реакций органической химии. Реакции, при которых валентность индексных атомов изменяется, мультиплетная теория не рассматривает. Развитые представления связаны с необходимостью ориентированной адсорбции молекул на поверхности катализатора. Наличие в индексной группе различных атомов, отличающихся межатомными расстояниями, обусловливает необходимость определенных межатомных расстояний на поверхности катализатора. Только при этих условиях ориентированная адсорбция индексной группы будет осуществляться с достаточной скоростью и с минимальным энергетическим барьером. [c.72]
Как видно из приведенного примера, даже в наиболее простой молекуле Li 2 строение МО является достаточно сложным. Свидетельством этому служит следующий факт. Экспериментально определенное межатомное расстояние Я в молекуле Ьц равно 0,267 нм. Если же рассчитать это расстояние, предполагая только а -связь (т. е. без участия 2р-орбиталей и других взаимодействий), то / = 0,278 нм, а при чистой яу-связи = 0,200 нм, т.е. даже небольшое участие 2р-орбитали в формировании химической связи способствует упрочнению молекулы. [c.295]
Методы рентгеновского и рентгеноэлектронного анализа широко используются [29, 30, 31] для изучения электронного строения атомов, молекул, а также зонной структуры твердых тел определения зарядового состояния атомов в молекулах и твердых телах установления элементного состава химических соединений (качественного и количественного анализа веществ) исследования химического и фазового состава поверхности и тонких пленок установления способа координации лигандов в комплексных соединениях изучения строения и природы ближнего окружения атомов в молекулах жидких и аморфных тел. Метод расширенного рентгеновского поглощения является уникальным по чувствительности методом структурного анализа твердых и жидких проб [32, 33]. Метод обеспечивает непосредственное определение межатомных расстояний даже в тех случаях, когда отсутствует кристаллографическая структура, позволяет решать проблемы дифференциации типа химической связи, расшифровки электронной геометрии молекул, оценки состояний окисления, в ряде случаев — исследования быстрых химических процессов. [c.172]
В случае гексагональной, моноклинной и триклинной структур определение межатомных расстояний усложняется, поскольку их система координат косоугольная, и в расчет входит угол между осями. [c.131]
Известно, что каждому типу связи приблизительно соответствует определенное межатомное расстояние. Так, если в большом числе структур алифатических соединений измерять расстояние С—С, то всегда будем получать величину, близкую к 1,54. Если же простая связь будет находиться между кратными, то величина ее может значительно уменьшиться за счет уменьшения кова- [c.367]
Определение межатомных расстояний [c.115]
Определение межатомных расстояний и диэдральных углов [c.137]
Лдя систем с количеством фаз больше одной применяется построение разностных кривых /»47. Точность определения межатомных расстояний- ЛУ у = + 0,5%, площадей пиков электронной плотности - [c.237]
Нами в ряде случаев на электронограммах от конденсированного германия были получены такие же диффузные максимумы, как и в работах [50]. Для определения межатомных расстояний мы пользовались приближенной формулой (стр. 81), но исследовали также и область от 1 до 2 А. Результат представлен на рис. 74. [c.139]
Существование довольно стойких радикалов и ионов типа приведенных в табл. 1 (например, производных трифенилметила) дало основание полагать, что такие частицы промежуточно образуются в тех случаях, когда они менее устойчивы. Наоборот, стабильные соединения формально двухвалентного углерода в этом отношении дают мало полезной информации. В окиси углерода, изонитрилах и в производных гремучей кислоты имеется очень сильное взаимодействие атомов двухвалентного углерода и связанных с ним групп. Определения межатомных расстояний, дипольных моментов и т. п. показали, что эти соединения существуют в основном в виде структур, содержащих тройные связи. Вследствие этого двухвалентный углерод в таких молекулах проявляет нуклеофильность. [c.10]
ПрЙ определении межатомных расстояний и геометрической конфигурации многоатомных молекул важное значение имеет электронография, особенно высокотемпературная (для неорганических молекул) [40. Интересный материал о геометрической конфигурации многих молекул получен с помощью метода, основанного на отклонении молекулярных пучков в неоднородном электрическом поле [41]. [c.21]
В этом соотношении А л В — константы, значение которых зависит от положения в периодической системе элементов, образующих связь. Определение межатомных расстояний таким методом проще, чем их вывод через моменты инерции из вращательных линий, проявляющихся в спектрах комбинационного рассеяния, так как эти линии в последних в большинстве случаев трудно наблюдаемы. [c.345]
Разработка методов определения межатомных расстояний также подтвердила правильность представлений химиков о существовании связей, качественно отличных от обычных простых и двойных связей. [c.53]
Исследовано старение аморфных окисей алюминия и его солей [156—1581 и некоторые свойства гидраргиллита [159—161]. Смитом [4421 показана возможность определения межатомного расстояния А1 — О. [c.301]
В настоящее время при исследовании строения органических веществ особенно широко используются электромагнитные колебания с длиной волны от миллиардных долей сантиметра до нескольких метров Дифракция рентгеновских лучей (Л = 0,1—0,01 10″ см) в кристаллах используется для определения межатомных расстояний и других параметров кристаллической решетки. Электромагнитные колебания ультрафиолетовой (Л = 10″ —4-10″ см), видимой (К = 4-1(Г<—7-10″ см) и инфракрасной = 7-Ю- -10- см) областей спектра используются для определения тонкого строения молекул. Микроволновые колебания (/ = 10 —10 см) характеризуют вращение молекул. Сантиметровые и метровые волны используются для определения строения органических соединений с одновременным воздействием на них электромагнитного поля (электронный парамагнитный и ядерный магнитный резонанс). [c.19]
В результате исследования вращательной структуры полос могут быть получены данные о симметрии молекулы. Например, простая тонкая структура вращательно-колебательных полос ацетилена свидетельствует о том, что молекула ацетилена является линейной. Кроме того, в простых молекулах по расстояниям между вращательными ли1шями могут быть определены мпмс ггы инерции, а отсюда может быть получено и межатомное расстояние, если в молекуле, например метана, имеется только одно такое расстояние. Когда в молекуле имеются два различных межатомных расстояния, как в ацетилене, для определения межатомных расстояний необходимо исследовать спектр поглощения двух изотопических форм (в данном случае С2Н2 и СаНО). Это позволяет найти два значения момента инерции, на основании которых могут быть вычислены необходимые расстояния. [c.307]
Однако спектральное определение межатомных расстояний и валентных углов возможно лишь в том случае, если измерена хорошо разрешенная тонкая структура ряда полос нескольких изотопных молекул и из нее определено столько различных моментов инерции, сколько имеется различных независимых межатомных расстояний и валентных углов у молекулы. Поэтому спектральное определение всех межатомных расстояний и валентныхуглов выполнено до сих пор лишь для следующих наиболее простых и симметричных молекул углеводородов метана, этана, этена, этина, бензола 8. Допуская, что полученные значения некоторых величин (длин связей С — Н и —С = С —, углов Н — С — Н) остаются неизменными, можно определить [c.482]
Структуры конденсированных сред можно группировать (классифицировать) по многим признакам. К сожалению, резкой границы между различными признаками нет и потому в любой классификации существует известный [5, 7] формализм. В настоящее время мы располагаем возможностью точного определения межатомных расстояний. По-видимому, этот признак (межато лное расстояние) и может быть прежде всего положен в основу классификации. Пользуясь этим признаком, все структуры- [71 делят на пять групп координационные, островные, цепочечные, слоистые, каркасные. [c.57]
Конформация. — В 1951 г. Полинг и Kopи предложили конформацию полипептидной цепи, в частности фибриллярных белков. Эта конформация в настоящее время подтверждена множеством доказательств. Основанием гипотезы Полинга и Кори были точные рентгеноструктурные определения межатомных расстояний в простых пептидах, таких, как L-aлa(Hил-L-aлalHИн, данные для которого представлены на диаграмме а. Вследствие резонанса пептидных групп связь С—N укорочена, а связь С = 0 удлинена, амидные группы лежат в одной плоскости в грамс-положении. [c.709]
Полученную таким способом систему атомных радиусов очень скоро пришлось оставить, так как обнаружилось большое количество противоречий, приведших к мысли о полной несостоятельности идеи, положенной в основу системы. В самом деле, радиус атома меди, определенный из структуры металлической меди, оказывается равным 1,27. Вычитая эту величину из найденного значения межатомных расстояний в структуре u l (2,35), получают для атома хлора радиус 1,08. Если проделать аналогичные определения размера атома хлора в структуре Na l, воспользовавшись размером атома натрия (1,86), определенного из структуры металлического натрия, то легко получить значение 0,95. Отклонение от предыдуш его значения для атома хлора превышает 0,15, что, конечно, недопустимо, так как точность определения межатомных расстояний даже в те годы была порядка [c.134]
Так как на величину оказывают влияние все спины исследуемой системы, то поведение намагниченности ядра А в принципе зависит от всей спиновой системы. Конечной целью исследования является определение, межатомных расстояний r j между атомами А и J. Можно показать, что изменение величины ЯЭО для очень малого времени смешивания 0) пропорционально. Для кросс-пика (точнее, объема кросс-пика) в спектре, полученном по методу NOESY, и для ЯЭО в одномерном экспери- [c.117]
Специфику процесса полимеризации можно попять при допущении, что на поверхности катализатора образуется новый координационный комплекс с участием мономера, в составе которого активированная мономерная молекула определенным образом ориентирована. Образование комплекса предшествует присоединению каждого очередного мономерного звена к растущей цепи. Такая схема полимеризации, которую следует отнести к анионнокоординационному типу, позволяет объяснить особенности алфиновых катализаторов, и в частности необходимость участия галогенида щелочного металла с определенным межатомным расстоянием. Очевидно, активные центры на поверхности катализатора и молекулы мономера должны находиться в строгом пространственном соответствии, что обеспечивает возможность образования первичного комплекса типа (I) или (II) [c.401]
В мультиплетной теории раньше всего была разработана секстетная модель дегидрогенизации шестичленных циклических углеводородов на металлических катализаторах. Эта модель передает много экспериментальных фактов, и, в частности, то, что катализаторами дегидрогенизации этого типа должны быть металлы с решеткой А1 и АЗ и с определенными межатомными расстояниями (от 1,22 до 1,39 А). Это широко-оправдалось на опыте [3] к таким катализаторам, действительно, относятся N1, Со, Си, КЬ, 1г, Р(1, Р1, Ки, Оз, 2п и Ке. Мультиплетная теория предсказала каталитическую активность рения для этой реакции. Секстетная модель затем подтвердилась в многочисленных исследованиях. Из них можно назвать следующие А. М. Рубинштейн, Н. И. Шуйкин и X. М. Миначёв [10] нашли, что каталитическая активность для этой реакции падает с уменьшением интенсивности рентгеновых отражений от граней (111) платины (на угле), что говорит о плоскостном расположении шестичленного кольца. Автор настоящего доклада и Г. В. Исагулянц [c.316]
При сопоставлении каталитической активности сплавов С11—N1, Си—Р , Си—Ад , Си—Аи, в реакциях гидрирования и окисления было достаточно убедительно показано [31, стр. 1313— 1315], насколько важны именно определенные межатомные расстояния в катализаторах такие расстояния имеются в упоря- [c.177]
Заметное расширение интерференционных колец, получаемых по методу Дебая — Шеррера, происходит в том случае, если размеры частиц лежат между 0,5—0,2 ц. Расширение колец закономерно возрастает с дальнейшим уменьшением размера частиц, что и делает возможным определение их величины. Это имеет место в том случае, если речь идет о кристалликах с совершенно правильным расположением в них атомов. Не вполне упорядоченное расположение атомов, т. е. существование так называемых искажений решетки (см. т. II, гл. 1), может также привести к расширению интерференционных колец и в случае значительно более крупных кристалликов. Будет ли это происходить, зависит от характера искажений. Существуют и такие искажения, которые обусловливают не расширение, но только уменьшение интенсивностей интерференционных колец. Более подробно см. F г i к е, Z. Ele tro hem., 44, 29, 1938> Так как в твердых аморфных, а также в жидких и газообразных веществах атомы располагаются не совершенно неупорядоченно, а определенные межатомные расстояния встречаются чаще других, то и для таких веществ наблюдаются более или менее отчетливые максимумы в почернениях фотографической пленки. Из положений этих максимумов можно сделать заключение о строении молекул. Для исследования молекулярной структуры таких веществ, и прежде всего газов, в настоящее время служат не только рентгеновские лучи, но и электронные лучи, которые при прохождении через газы преломляются и испытывают интерференции таким же образом, как и рентгеновские лучи. [c.236]
В катализе встречаются матрицы разных типов и размеров. Особенно велико их многообразие в гетерогенном катализе и в катализе макромолекулами полимеров. Но матрица в катализе — это не чисто геометрическое понятие. Для того чтобы определенная матричная структура могла осуществлять свои функции, ее структурные элементы должны обладать должным образом распределенной реакционной способностью. А это уже проявление тонких электронных свойств, без чего геометрия бесполезна. Данный факт не учитывается в традиционной концепции геометрического соответствия Баландина [50] и в фишеровской модели ключа и замка для ферментативного катализа. Такие концепции нуждаются в модернизации и в существенных коррективах. Так, в основу теории мультиплетов положено представление о точном совпадении определенных межатомных расстояний и элементов симметрии определенных граней кристаллов, образующих гранулы катализатора, с расстояниями между атомами в реагирующих молекулах и с их геометрической структурой. Постулируется дуплетная, тршлетная, квадру- и секстетная адсорбция реагентов с образованием химических связей с двумя, тремя, четырьмя и шестью атомами (ионами) решетки. Природа этих связей остается неопределенной. Секстетная модель, в частности, применяется для адсорбции циклогексана и бензола на Р1, №, Рс1, Со и других переходных металлах, катализирующих дегидрирование и гидрирование, как это показано на рис. 1.17. В этой концепции имеется несколько слабых мест. [c.37]