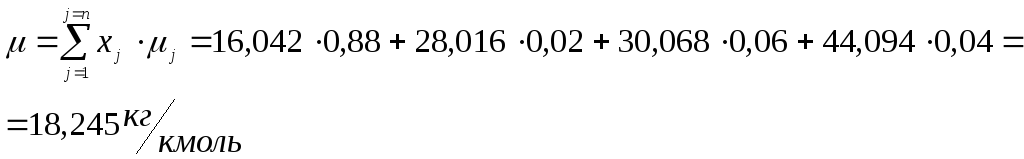Газовая постоянная, справочная таблица
| Азот газовая постоянная азота |
297 (Джоуль / (Килограмм · Кельвин)) |
| Аммиак газовая постоянная аммиака |
488 (Джоуль / (Килограмм · Кельвин)) |
| Аргон газовая постоянная аргона |
208 (Джоуль / (Килограмм · Кельвин)) |
| Ацетилен газовая постоянная ацетилена |
320 (Джоуль / (Килограмм · Кельвин)) |
| Бутан газовая постоянная бутана |
143 (Джоуль / (Килограмм · Кельвин)) |
| Водород газовая постоянная водорода |
4125 (Джоуль / (Килограмм · Кельвин)) |
| Водяной пар (100°C) газовая постоянная водяного пара |
461 (Джоуль / (Килограмм · Кельвин)) |
| Воздух газовая постоянная воздуха |
287 (Джоуль / (Килограмм · Кельвин)) |
| Гелий газовая постоянная гелия |
2078 (Джоуль / (Килограмм · Кельвин)) |
| Двуокись углерода газовая постоянная углекислого газа |
189 (Джоуль / (Килограмм · Кельвин)) |
| Кислород газовая постоянная кислорода |
260 (Джоуль / (Килограмм · Кельвин)) |
| Метан газовая постоянная метана |
519 (Джоуль / (Килограмм · Кельвин)) |
| Неон газовая постоянная неона |
412 (Джоуль / (Килограмм · Кельвин)) |
| Окись углерода газовая постоянная угарного газа |
297 (Джоуль / (Килограмм · Кельвин)) |
| Пропан газовая постоянная пропана |
189 (Джоуль / (Килограмм · Кельвин)) |
| Пропилен газовая постоянная пропилена |
198 (Джоуль / (Килограмм · Кельвин)) |
| Фреон газовая постоянная фреона |
68.7 (Джоуль / (Килограмм · Кельвин)) |
| Этан газовая постоянная этана |
277 (Джоуль / (Килограмм · Кельвин)) |
| Этилен газовая постоянная этилена |
297 (Джоуль / (Килограмм · Кельвин)) |
Газовая постоянная — справочная таблица |
стр. 862 |
|---|
Дисциплина:
СООРУЖЕНИЕ И ЭКСПЛУАТАЦИЯ ГАЗОНЕФТЕПРОВОДОВ
И ГАЗОНЕФТЕХРАНИЛИЩ
Раздел: ХРАНЕНИЕ
НЕФТИ, ГАЗА И НЕФТЕПРОДУКТОВ
Практическое
занятие № 6
вычисление
физических характеристик свойств
природных газов в зависимости от внешних
условий
Указания
к выполнению задания
Природный
газ состоит в основном из метана
.
Плотность
газа зависит от его состава, давления
и температуры. При стандартных
условиях
(
= 0,1013 МПа,
= 293 К) плотность природного газа
составляет примерно 0,7 кг/м3.
Относительной
плотностью
газа по
воздуху
называется отношение
плотности
природного газа к плотности
воздуха при одних и тех же (например,
стандартных) условиях. Очевидно, что
для совершенных газов это отношение не
зависит ни от давления, ни от температуры.
В частности, плотность
природного газа представляется в виде:
,
причем
.
Связь
вида
между давлением
в газе, его удельным объемом
и абсолютной температурой
называется уравнением
состояния
газа. При умеренных давлениях и
температурах свойства газов достаточно
хорошо моделируются уравнением состояния
Клапейрона-Менделеева:
(101)
где
— объем газа;
— его масса;
— молярная масса газа, (кг/кмоль);
— универсальная газовая постоянная
().
Газы, свойства которых моделируются
уравнением Клапейрона-Менделеева,
называют совершенными.
Если
учесть, что удельный объем
газа определяется как
,
и
— газовая постоянная данного
газа, то уравнение состояния совершенного
газа записывается также в форме:
или
.
(102)
Газовая
постоянная
метана равна 518,33 Дж/(кг• К), углекислого
газа — 188,95 Дж/(кг • К ), кислорода — 259,8 1
Дж/(кг • К ), воздуха — 287,1 Дж/(кг• К);
.
Свойства
реальных природных газов отличаются
от свойств совершенного газа.
Для каждого реального газа имеется
некоторая критическая
температура
такая, что для любого значения
существует давление
,
при котором происходит фазовый переход
газа в жидкое состояние, а для температур
такой переход невозможен ни при каких
давлениях. Если
,
то существует давление
,
при котором свойства жидкой и газовой
фаз неразличимы. Параметры газа
называется критическими.
Так, например, для метана эти параметры
составляют:
.
Некоторые постоянные
компонентов, составляющих природный
газ, приведены в нижеследующей таблице.
Таблица
Постоянные
компонентов, составляющих природный
газ
|
Газ |
Молярная масса, |
Плотность по |
Критическое |
Критическая |
|
Метан |
16,042 |
0,554 |
4,641 |
190,55 |
|
Этан |
30,068 |
1,049 |
4,913 |
305,50 |
|
Пропан |
44,094 |
1,562 |
4,264 |
369,80 |
|
Изобутан |
58,120 |
2.066 |
3,570 |
407,90 |
|
н |
58,120 |
2,091 |
3.796 |
425.17 |
|
н |
72,146 |
2,480 |
3,374 |
469,78 |
|
Азот |
28,016 |
0,970 |
3,396 |
126,25 |
|
Кислород |
32,000 |
1,104 |
4,876 |
154,18 |
|
Сероводород |
34,900 |
1,190 |
8,721 |
373.56 |
|
Углекисл.газ |
44,011 |
1,525 |
7,382 |
304,19 |
|
Водород |
2,020 |
0,069 |
1,256 |
33,10 |
|
Гелий |
4,000 |
1,136 |
0,222 |
5,00 |
|
Воздух |
28,966 |
1,000 |
3,780 |
132,46 |
В ряде случаев
уравнение состояния реального газа
представляют в виде
(103)
где
— безразмерный коэффициент
сжимаемости
газа (называемый иногда еще коэффициентом
сверхсжимаемости
газа). Очевидно, что для совершенных
газов
.
Зависимость
от отношений
и
,
называемых приведенным
давлением
и приведенной
температурой,
соответственно, представлена на рис.
1.12.
Рис.
1.12. Зависимость
от
и
.
Для
природных газов, представляющих собой
метан в смеси с некоторыми другими
компонентами (этан, пропан, бутан,
изо-бутан, пентан, азот, сероводород,
углекислый газ, водород, гелий и т.п.),
коэффициент
сжимаемости может быть рассчитан по
следующей аппроксимационной формуле:
(104)
Молярная масса и
критические параметры газовой смеси
вычисляются по следующим аддитивным
формулам:
;
;
(105)
где
— объемные доли компонентов, составляющих
газ.
Простейшие
термодинамические процессы.
Изотермический
процесс:
.
При изотермическом расширении (или
сжатии) совершенного газа от давления
до давления
к газу необходимо подводить (или
соответственно отбирать) тепло:
(106)
где
— количество тепла, рассчитанное на
единицу массы газа (Дж/кг или кал/кг;
1кал = 4,187 Дж); причем
,
если газ расширяется (),
и
,
если газ сжимается ()
Обратимый
адиабатический
процесс:
.
Имеют место следующие соотношения:
,
(107)
где
— плотность, давление и температура газа
в начальном состоянии;
— те же параметры газа в текущем (или
конечном) состоянии;
— показатель адиабаты;
— теплоемкости газа соответственно при
постоянном давлении и объеме (Дж/(кг К).
Например, для воздуха
;
для метана —
;
для этана —
;
для пропана
и т.д. Для совершенного газа ()
имеет место формула Майера:
.
Политропическим
называется
процесс, в котором плотность и давление
связаны уравнением:
,
где
;
— показатель политропы. Если в этом
процессе
,
то
.
Если процесс политропического сжатия
газа ()
идет с подводом тепла (),
то
;
если же он сопровождается отбором тепла
(),
то
.
В политропическом
процессе плотность, давление и температура
газа связаны соотношениями, аналогичными
(107):
т-1
,
(108)
Примеры
решения задач
Задача
1
Газовая смесь
состоит из 99 % метана, 0,5 % этана и 0,5 %
азота. Определить молярную массу газовой
смеси и значение газовой постоянной.
Решение
Задачи 1.
-
Рассчитаем
молярную массу по формуле:
-
Рассчитаем
значение газовой постоянной смеси:
Задача
2
Газовая смесь
состоит из 88 % метана, 6 % этана, 4% пропана
и 2 % азота. Определить молярную массу
газовой смеси и значение ее газовой
постоянной.
Решение
Задачи 2.
-
Рассчитаем
молярную массу по формуле:
-
Рассчитаем
значение газовой постоянной смеси:
Задача
3
Определить
массу 100 тыс. стандартных (то есть
вычисленных при давлении р = 0,1013 МПа и
температуре Т = 293 К) кубометров природного
газа (
= 19,2 кг/кмоль).
Решение
Задачи 3.
-
Рассчитаем
массу по формуле Менделеева-Клайперона:
→
Задача
4
Объем
природного газа, измеренный при
стандартных условиях, составляет 10 тыс.
м3.
Каков объем этого газа при нормальных
(то есть вычисленных при давлении р =
0,1013 МПа и температуре Т = 273 К) условиях?
Решение
Задачи 4.
-
Запишем
уравнения Менделеева-Клайперона для
нормальных и стандартных условий:
-
Совместно
решим уравнения (1):
Задача
5
Природный
газ, хранящийся в резервуаре емкостью
20 тыс. м3
при среднем давлении 0,11 МПа, подвержен
колебаниям суточной температуры от +8
°С ночью до +20 ˚С днем. Определить
амплитуду колебания давления в резервуаре.
Решение
Задачи 5.
-
Запишем
уравнения Менделеева-Клайперона для
дневных и ночных условий:
-
Совместно
решим уравнения (1):
-
Известно,
что:
-
Совместно
решим уравнения (2) и (3):
-
Суточные
колебания давления составят:
Задача
6
Газовую
полость (или газовый пузырь) подземного
хранилища газа (ПХГ) можно приближенно
считать прямым цилиндром, имеющим в
плане форму прямоугольника со сторонами
a
= 3770 м, b
= 5000 м и высотой h
= 15 м. Пористость m
пласта (то есть объемная доля пустот в
породах, слагающих пласт), составляет
30 %. Насыщенность s
пустот газом (то есть объемная доля этих
пустот, заполненных газом), равна 0,65;
остальная часть пустот заполнена водой.
Определить, какой объем газа в стандартных
кубических метрах находится в ПХГ, если
известны пластовое давление р = 10 МПа и
температура Т = 30˚С газа. Известны также
постоянные газа: R
= 470 Дж/(кг К), ркр
= 4,7 МПа, Ткр
= 200 К.
Решение
Задачи 6.
-
Определим
поровый объём газа Vп:
-
Определим
коэффициент сжимаемости газа Z:
-
Определим
плотность газа в пластовых условиях:
-
Определим
массу газа M:
-
Определим
плотность газа при стандартных условиях
:
-
Определим
объём газа, выраженный в стандартных
кубических метрах:
Соседние файлы в папке практика 6
- #
- #

Таблицы DPVA.ru — Инженерный Справочник
Адрес этой страницы (вложенность) в справочнике dpva.ru: 
Индивидуальные газовые постоянные и молярные массы некоторых газов Ri. Азот, Аргон, Водяной пар, Водород, Воздух, Гелий, Диоксид серы , Кислород, Метан, Пропан, Углекислый, Угарный газ
|
||||||||||||||||||||||||||||||||||||||||
|
Поиск в инженерном справочнике DPVA. Введите свой запрос: |
Поиск в инженерном справочнике DPVA. Введите свой запрос:
Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста.
Вложите в письмо ссылку на страницу с ошибкой, пожалуйста.
Коды баннеров проекта DPVA.ru
Начинка: KJR Publisiers
Консультации и техническая
поддержка сайта: Zavarka Team
Free xml sitemap generator
2.18 Найти газовую постоянную для кислорода, водорода и метана (СН4).
Ответ: RO2=259,8 кДж/(кг·К), RН2=4124 кДж/(кг·К), RСН4=518,6 кДж/(кг·К).
В корзину – 100 RUB