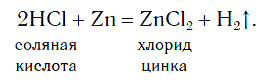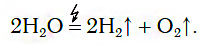Водород давно и довольно широко используется в химической и пищевой промышленности, в нефтепереработке. Но как об энергоресурсе о водороде заговорили сравнительно недавно. Первые экспериментальные проекты использования этого газа в качестве топлива для транспорта появились в начале текущего века. На протяжении двух десятилетий «водородный тренд» постепенно набирал силу. В широкое употребление вошло понятие «водородная экономика». Планы её развития, заявленные в ряде стран, включая Россию, подразумевают многократное увеличение производства и потребления водорода в энергетических целях — в качестве топлива, для производства электрической и тепловой энергии.
Электролизная станция с ресиверами хранения водорода. Березовская ГРЭС. Красноярский край (2014 год). Фото Валерия Акулича/Фотобанк Лори.
В результате риформинга получается синтез-газ (другое название — водяной газ) — газовая смесь, основные компоненты которой CO и H2. Выход водорода увеличивается в результате конверсии CO при взаимодействии с водяным паром (так называемая реакция водяного газа). Но при этом образуется углекислый газ. Возможна модификация процесса, включающая частичное улавливание и захоронение двуокиси углерода. Если процесс идёт без улавливания двуокиси углерода (А), стоимость получения 1,1 т водорода составляет 590 долл. США (в ценах 2019 года). В процессе с частичным улавливанием и захоронением двуокиси углерода (Б) стоимость получения 1,1 т водорода — 1091 долл. США. Такой процесс нельзя считать ни дешёвым, ни экологически чистым. Рисунок: Parent55/Wikimedia Commons/CC0 (с изменениями).
Процесс не сопровождается образованием парниковых газов — то есть это экологически чистый процесс, но пока он остаётся весьма энергоёмким и очень дорогим. По данным Управления энергетической информации США (USEIA) 2019 года, производство примерно 1 т водорода обходится в 1,497 долл. США. Рисунок: Parent55/Wikimedia Commons/PD (с изменениями).
Водород долгое время хранили в сжатом либо жидком виде. Жидкий водород требует специального «криогенного» хранения (то есть в теплоизолированных контейнерах) и особого обращения из-за опасности взрыва. На фото огромный сосуд с жидким водородом в экспериментальной вакуумной камере в Исследовательском центре Льюиса (теперь Исследовательский центр Джона Гленна — John Glenn Research Center, NASA), 1967 год. Фото: NASA/GRC/Paul Riedel, Lloyd Trunk/Wikimedia Commons/PD.
Канадская компания по бурению газовых скважин в 2017—2018 годах в поисках углеводородов пробурила несколько скважин неподалёку от селения Буракебугу (Мали). Перед бурением специалисты компании провели геохимический мониторинг почвы в различных точках исследуемого участка. Результаты оказались неожиданными: примерно на глубине 1 м была обнаружена высокая концентрация водорода. В ходе дальнейших работ компания выявила пять крупных пластов залежей водорода. Каждый резервуар был покрыт слоем долерита — магматической горной породы, аналога базальта. Общая площадь пластов запасов водорода оценили в 780 км2. На снимке показана впадина с повышенным содержанием в почве водорода, расположенная к востоку от участка, где проводила работу канадская компания, и профиль концентрации водорода в разных точках впадины. Иллюстрация из статьи: Prinzhofer A., Tahara Cissé C. S., Diallo A. B. Discovery of a large accumulation of natural hydrogen in Bourakebougou (Mali) // International Journal of Hydrogen Energy, V. 43, Is. 42, 2018, pp. 19315—19326.
Мезосферные, или серебристые, облака возникают на высотах 70—95 км. На таких высотах концентрация паров воды слишком низка для образования облаков, однако теоретически вода могла бы образовываться при взаимодействии водорода с кислородом. На снимке: серебристые облака в небе над Якутией, июль 2021 года. Фото Петра Андреева/Wikimedia Commons/CC BY-SA 4.0.
‹
›
Предполагается, что водород наряду с возобновляемыми источниками энергии вытеснит «традиционные» углеводородные энергоносители. Водород активно позиционируют в качестве экологически безопасного «углеродно-нейтрального» источника энергии, а планируемый рост его производства и использования — как движение по пути декар-бонизации мировой экономики и снижения потребления ресурсов. Под декарбонизацией понимается прекращение выбросов углерода и его соединений, прежде всего углекислого газа CO2, антропогенную эмиссию которого рассматривают в качестве одной из ключевых причин глобального потепления. Но с возможностью перевода энергетики на водород не так всё просто.
Лёгкий, горючийи очень теплотворный
Наверное, каждому из школьного курса химии известно, что водород — первый химический элемент таблицы Менделеева. Есть ряд изотопов водорода, но основной из них — протий (1H), на который приходится примерно 99,99% атомов водорода на Земле и во Вселенной. Ядро протия состоит всего из одного протона. Как следствие, это самый лёгкий химический элемент. Для сравнения, при нормальном атмосферном давлении 1 м3 воздуха имеет массу около 1,2 кг, 1 м3 природного газа (метана CH4) — 700 г, а 1 м3 газообразного водорода (химическая формула H2) — всего 90 г. То есть водород почти в 8 раз легче природного газа и в 13 раз легче воздуха.
Водород бесцветен, не имеет запаха, при этом он химически активен, горюч и взрывоопасен. Но его горение действительно не даёт выбросов загрязнителей атмосферы. Реакция горения водорода идёт с образованием воды, с выделением большого количества энергии E (тепла): 2 H2 + O2 =>2H2O + E. То есть это тепло — экологически чистая энергия.
Водород — самый распространённый элемент во Вселенной, на него приходится почти 89% общего числа её атомов и около 75% её массы, поскольку этот газ — основное вещество звёзд и топливо для их «работы». Отметим, что остальные 11% атомов Вселенной приходятся на гелий — собственно, продукт «горения» звёзд, и только 0,1% — на все остальные химические элементы.
Однако в обитаемом и доступном нам мире водорода на порядки меньше. Например, в земной коре его содержание оценивается всего в 1% по массе и около 17% — по общему количеству атомов. В земной атмосфере водород также выглядит исчезающе малой величиной — 5•10-5% (0,00005%) общего объёма атмосферы и 3,5•10-6% (0,0000035%) её массы. При этом свободного водорода на Земле мы почти не видим. Слишком лёгкий элемент в атмосфере плохо удерживается земным притяжением, но охотно вступает в химические реакции, образуя разные соединения, в которых он в основном и присутствует в географической оболочке.
Самое распространённое соединение водорода — вода, а самый большой на Земле резервуар этого газа — Мировой океан, на который приходится 96% воды на планете. Объём и масса вод Мирового океана — огромные величины: более 1,3 млрд км3 и, соответственно, 1,3•1018 т. На водород в массе воды приходится 11%, то есть, в океанической воде его содержится примерно 1,4•1017 т, и ещё приблизительно 5,6•1015 т — в остальных водах Земли. Это в совокупности очень немного относительно массы земной коры, составляющей 2,8•1019 т, — примерно полпроцента.
Оценим это количество водорода в энергетических единицах, сопоставляя с потребностями человечества. Теплотворная способность данного газа — 3,6 кВт•ч/м3, или 40 кВт•ч/кг и 40 МВт•ч/т. Это примерно в три раза выше, чем у природного газа. Иными словами, только в пресных водах Земли (это всего 4% от всей земной воды) содержится 2,24•1017 МВт•ч, или 2,24•1011 ТВт•ч потенциальной водородной энергии. Для сравнения, вся энергия, потребляемая человечеством в течение года, менее 2•105 ТВт•ч1 — в миллион раз меньше. И нужно «всего» 5 млрд тонн водорода в год, чтобы обеспечить энергией всё человечество на текущем уровне. При этом в пресной воде Земли его больше в 1 млн раз, а в океанической — в 25 млн раз.
Огромное по сравнению с нуждами мирового энергопотребления количество водорода в виде его соединений содержится в запасах угля, нефти и газа, собственно, и называемых углеводородным сырьём. Дать точную цифру мировых ресурсов ископаемых углеводородов невозможно, но на данный момент только разведанные запасы в совокупности превышают 1 трлн тонн, и водорода в них не менее 100 млрд тонн, при этом на Земле разведано далеко не всё и ресурсная база постоянно пополняется.
Иными словами, теоретически, если мы начнём использовать водород в качестве топлива для выработки тепловой и электрической энергии, извлекая его только из воды, нам хватит его как энергоносителя на десятки миллионов лет, то есть навсегда.
Желанный,но такой дорогой
Почему же до сих пор водород не стал энергоносителем номер один?
Два главных способа получения этого газа в настоящее время — конверсия углеводородного сырья и электролиз воды. Но извлечение водорода из его соединений означает разрыв химических связей между водородом и кислородом в случае воды или между углеродом, кислородом и водородом в случае углеводородов. И оба процесса сопряжены с очень большими затратами энергии, с дорогостоящим оборудованием и, заметим, с загрязнением окружающей среды.
В настоящее время в мире производится около 75 млн т водорода в год, и пока его производство растёт невысокими темпами — менее 2% в год. При этом из углеводородного сырья добывается более 90% всего производимого водорода, в том числе 70% — с помощью конверсии природного газа, самого доступного способа. В основе процесса — подвод к природному газу тепла (нагрев печи до 600—1000°С) и водяного пара в присутствии металлического катализатора — кобальта, никеля, железа. Это самый дешёвый, но экологически грязный способ, оставляющий большой углеродный след, то есть выбросы CO2 в атмосферу. Он описывается химическими реакциями:
CH4 + H2O = CO + 3H2
СО + H2O = CO2 + H2
На выходе, как можно видеть, — большое количество углекислого газа. Кроме того, при расчёте стоимости процесса надо учитывать не только затраты собственно на работу печи, но и на добычу и транспортировку газа. И если рассматривать водород как топливо, то дешевле и экологически чище просто добывать и сжигать природный газ.
Есть и другие способы углеводородной конверсии — например, газификация и пиролиз угля и даже получение водорода из биомассы, но углеродный след и высокие затраты присущи всем этим решениям.
Если слегка коснуться цифр, то стоимость производства водорода методами углеводородной конверсии оценивается от $2 за 1 кг. Один лишь расход метана на производство 1 кг водорода составляет 5 м3, а при угольной конверсии производство 1 кг водорода потребует более 6 кг угля. Цена, очевидно, высока, при этом использование водорода как энергоносителя с КПД, равным 100%, невозможно, и количество полученной энергии в данном случае надо делить примерно на два—три. Добавим ещё затраты на создание и поддержание инфраструктуры для транспортировки и хранения водорода и получим исключительно дорогое топливо, производство которого далеко не безупречно с экологической точки зрения.
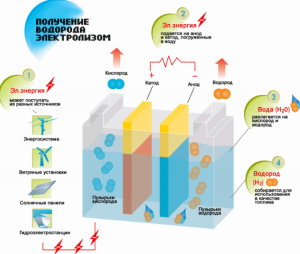
Остаётся единственный экологически чистый способ получения водорода — извлечение его из воды, которой на Земле намного больше, чем углеводородного сырья, и она, очевидно, доступнее. Самый распространённый способ получения водорода из воды — электролиз, то есть разложение воды под действием электрического тока:
2H2O = 2H2 + O2
Побочный продукт электролиза — только кислород, однако этот процесс исключительно энергоёмкий. Для получения 1 кг водорода (напоминаем, теплотворная способность такого количества газа при 100%-ном КПД составит около 40 кВт•ч) нужно затратить 40—50 кВт•ч электроэнергии. Таким образом, расход энергии оказывается больше (а с учётом реальной эффективности использования конечного продукта — минимум вдвое больше), чем энергия, полученная на выходе. Что касается денежного эквивалента, то затраты на производство водорода путём электролиза оцениваются в $3—7 за 1 кг, что существенно выше, чем при конверсии углеводородов. И электролизом воды получают лишь 2% производимого водорода.
Другая проблема — собственно, источник электроэнергии для ведения электролиза. Пока около 63% всей производимой в мире электроэнергии вырабатывается на угольных и газовых теплоэлектростанциях. Причём это соотношение не изменилось за последние 30—40 лет. Да, доля таких возобновляемых источников энергии, как ветер и солнце, ощутимо растёт, но происходит это в большей степени за счёт снижения доли атомной и гидроэнергии, а не ТЭС. Поэтому на данный момент использование водорода в качестве топлива, полученного посредством электролиза воды, не приводит к снижению выбросов углерода в атмосферу, просто эти выбросы идут не с электролизных установок, а с электростанций, поставляющих им энергию.
По-настоящему «зелёным» водородом можно считать только тот, производство которого не связано с выбросами углерода, то есть если для его получения используется электроэнергия от возобновляемых источников: гидростанций, ветровых, солнечных, приливных, геотермальных станций. Однако и этот водород остаётся дорогим.
Но, несмотря на комплекс проблем — экономических, энергетических, экологиче-ских, — в последние годы в мире активно заговорили об использовании водорода в качестве транспортного топлива, источника тепловой и электроэнергии. Сейчас примерно половина производимого водорода идёт на получение аммиака, расходуемого большей частью для производства азотных удобрений. Кроме того, водород используется для получения метанола, в нефтепереработке, пищевой и косметической промышленности. И всего доли процента этого газа идут на энергетическое обеспечение.
Строительствоводородной утопии?
В 2017—2020 годах ряд стран приняли масштабные водородные программы (которые, правда, пока носят декларативный характер), предполагающие многократный рост потребления водорода с перспективами его использования в энергетических целях и, соответственно, с кардинальным увеличением его доли в энергобалансе.
В частности, Евросоюз в 2019 году опубликовал дорожную карту развития водородной экономики (Hydrogen Roadmap Europe). Согласно изложенному в ней сценарию, общее потребление водорода в качестве энергоносителя в странах ЕС должно к 2050 году вырасти почти в 8 раз с нынешних примерно 300 ТВт•ч (это 2% в общей структуре потребления энергии) до 2250 ТВт•ч, или 24%.
В Японии аналогичная дорожная карта (Strategic Roadmap for Hydrogen and Fuel Cells) предполагает рост объёмов использования водорода к 2050 году до 10 млн т в год.
Всего в мире заявлено уже более 200 водородных проектов на всех континентах, большей частью в Западной Европе и Восточной Азии.
По самым смелым прогнозам (вероятно, ориентирующимся на европейскую дорожную карту развития водородной экономики), к 2050 году в мире на водород придётся 24% всей потребляемой энергии — это около 40 000 ТВт•ч, что потребует производства до 2 млрд т этого газа в год — примерно в 20 раз больше, чем в настоящее время.
В России в августе 2021 года также была принята Концепция развития водородной энергетики, предполагающая создание трёх-четырёх водородных кластеров, или центров производства и использования водорода: Северо-Западного, Восточного, Арктиче-ского и, возможно, Южного. При этом три из них — Северо-Западный, Восточный и Южный — ориентированы главным образом на внешние рынки. Предполагается увеличение экспорта водорода до 0,2 млн т к 2024 году и до 2 млн т — к 2035 году. Из конкретных проектов пока можно назвать только создание Сахалинского водородного кластера.
По данным, приведённым в Концепции, текущий ежегодный мировой спрос на водород составляет 116 млн т, в том числе на чистый водород — 74 млн т и 42 млн т — на водород в смеси с другими газами в качестве сырья или топлива для производства тепловой и электрической энергии.
У России есть конкурентные преимущества: наличие энергетического потенциала в сочетании с большим объёмом недозагруженных мощностей; большой опыт производства водорода и развитая научно-техническая база; выгодное географическое положение — близость территорий с высоким энергетическим потенциалом (в том числе — возобновляемых источников энергии) к западноевропейскому и восточноазиатскому рынкам сбыта. Тем не менее принятая Концепция выглядит как реакция на мировой водородный тренд и стремление встроиться в него главным образом в качестве экспортёра — по аналогии с экспортом других энергоносителей, которые мы в настоящее время поставляем на мировой рынок. Действительно, обнародованные Западной Европой и Японией грандиозные водородные планы потребуют импорта водорода, поскольку собственных мощностей для его производства в заявленных объёмах у них просто не хватит. Чтобы убедиться в этом, можно обратиться к некоторым цифрам.
По данным Международного энергетического агентства и других организаций, ведущих энергетическую статистику, годовой объём производства электроэнергии сейчас в странах ЕС — менее 4000 ТВт•ч, из которых на возобновляемые источники, включая гидроэнергию, в 2019 году приходилось около 1500 ТВт•ч, или 38%. При этом, как сказано выше, к 2050 году, согласно амбициозным планам ЕС, водород должен давать более 2000 ТВт•ч энергии. То есть, если даже все электростанции ЕС, работающие на возобновляемых источниках, будут задействованы исключительно для производства водорода, их мощностей не хватит для реализации подобных планов. Аналогичная ситуация в Японии. Производство заявленных 10 млн т водорода в год потребует более 400 ТВт•ч электроэнергии. Но сейчас в Японии вырабатывается всего чуть более 1000 ТВт•ч, из них 200 ТВт•ч, или около 20%, на основе возобновляемых источников, включая ГЭС. Что касается газа и угля, то достаточных запасов у Европы и Японии тоже нет. Кроме того, как использование ископаемого горючего для производства водорода согласуется с курсом на декарбонизацию? Выходит, странам с большими водородными планами надо многократно наращивать мощности электростанций, работающих на возобновляемых источниках (что вряд ли возможно в случае Западной Европы или Японии), или импортировать водород. Второй вариант уже задействован в Японии. С 2019 года осуществляется проект поставок туда сжиженного водорода танкерами из Австралии. Но этот водород производится в Австралии из бурого угля. Вопрос тот же: а как же декарбонизация и борьба с глобальным потеплением?
Получается, что строительство водородной экономики возможно благодаря странам с богатыми углеводородными ресурсами и с менее жёстким подходом к экологии. Но в таком случае нет смысла говорить о сокращении эмиссии углерода и нельзя рассматривать переход на водородное топливо как путь к декарбонизации: в лучшем случае декарбонизация в одних точках земного шара будет следствием «карбонизации» на других территориях.
В России возможности для налаживания производства и экспорта водорода связаны не только с угольными и газовыми ресурсами, но и с развитой гидро- и атомной энергетикой, а также растущими мощностями солнечной и ветровой энергетики. В отдалённой перспективе возможна выработка водорода и на приливных электростанциях.
Добавим, что обсуждается целесообразность строительства трёх мощных приливных электростанций — Мезенской на Белом море, Тугурской и Пенжинской в заливах Охотского моря. Речь идёт об активизации работы над проектами приливных станций, начатой ещё в советское время. Сейчас они рассматриваются в контексте дешёвой и экологически чистой выработки водорода и аммиака и их экспорта в Западную Европу и Восточную Азию.
В то же время хотелось бы, чтобы увеличение производства водорода у нас было ориентировано в большей степени на соб-ственное технологическое и экономическое развитие, нежели чем на появление новой статьи экспорта энергоресурсов.
В мире, как мы видим, в отношении строительства водородной экономики, тем более под флагом декарбонизации и вообще заботы об экологии, есть ряд нерешённых вопросов и противоречий, связанных и с технологиями, и со стоимостью производ-ства водорода. По-видимому, в связи с этим в последние несколько лет заговорили об аммиаке как потенциальной замене водорода в качестве топлива. Анонсировано несколько проектов масштабного производства аммиака, например, в Саудовский Аравии и Австралии. В качестве топлива аммиак действительно имеет ряд преимуществ по сравнению с водородом. Прежде всего, этот газ «компактнее»: плотность газообразного аммиака при нормальных температуре и давлении — 0,78 кг/м3, что почти в девять раз выше, чем у водорода. Также аммиак проще хранить и в жидком виде: температура кипения аммиака 33°С, тогда как у водорода -252°С. Аммиак может выступать и в качестве самостоятельного топлива, и как своего рода аккумулятор, хранилище водорода. Однако получение аммиака сложнее, дороже и связано с ещё большими экологическими издерж-ками, чем производство водорода, — хотя бы потому, что для его производства сначала надо извлечь водород, а уже потом — соединить его с азотом.
Таким образом, ожидания быстрого перехода на водородное топливо выглядят явно завышенными. В то же время у водорода действительно есть энергетические перспективы. Прежде всего, он интересен как аккумулятор энергии, поэтому водородная энергетика может помочь развитию энергетики, основанной на возобновляемых источниках. Их главная (хорошо известная) проблема — нестабильность, с чем уже сталкиваются страны, где возобновляемые источники энергии заняли достаточно большую долю в энергобалансе. При этом аккумуляция энергии в пиковые периоды с тем, чтобы расходовать её во время энергетического дефицита, — задача пока не решённая, тем более на длительных временных интервалах, на уровне сезонов. Например, в высоких широтах, даже на широте Москвы, поступление солнечной энергии летом не уступает таковому в тропических и экваториальных широтах, да и у Полярного круга в середине лета солнечной энергии почти столько же, сколько в тропиках. Но зимой её в десятки раз меньше в средней полосе, тем более — в полярных зонах, где она практически отсутствует и солнечные батареи бездействуют. Очевидно, что в данном случае для эффективной работы солнечной энергетики необходимы системы её аккумуляции. Примерно то же можно сказать и о гидроэнергии, и о ветровой энергии — сила их энергетических потоков меняется на порядки в зависимости от сезона. Преобразование энергии в водород путём электролиза в период, когда её «некуда девать» и она, условно говоря, бесплатна, и последующее использование запасённого водорода в период недостаточного поступления энергии из возобновляемых источников выглядит эффективным и экологически чистым решением проблемы.
Системы аккумуляции водорода могут быть различными. Помимо упомянутого выше аммиака очень удобный, недорогой и компакт-ный способ хранения — в форме гидридов. Подобными разработками активно занимается, в частности, Лаборатория водородных энергетических технологий Объединённого института высоких температур РАН.
Другой перспективный вид использования водорода — топливные водородные элементы для транспорта. Они обладают высоким КПД, существенно превосходящим КПД двигателей внутреннего сгорания, а их стоимость с развитием технологий снижается, хотя пока автомобили на водороде остаются слишком дорогими для потребителей. Кроме того, может возникнуть конкуренция между водородным и электротранспортом. Уже сейчас проводятся сравнения целесообразности того и другого с технологической, экономической и экологической позиций.
В поисках свободного водорода
Выше мы говорили о том, что главная проблема становления водородной экономики — почти полное отсутствие в зоне нашей досягаемости свободного водорода. Но так ли это на самом деле?
Чтобы ответить на этот вопрос, начнём с фундаментального и, на первый взгляд, лишённого явной практической значимости вопроса о составе земного ядра. Согласно хрестоматийной схеме, оно железное, но достаточно давно высказывались предположения, в том числе В. И. Вернадским и другими исследователями ещё прошлых веков, о росте количества водорода с глубиной и, как следствие, возможностях выходов свободного водорода на земную поверхность. Предполагается, что наиболее активные выходы водорода — в рифтовых зонах. Также существует концепция гидридного, то есть состоящего из соединений водорода с металлами, ядра Земли, которую обосновал советский геолог Владимир Николаевич Ларин ещё в1970-е годы. Он провёл сравнительный анализ распространённости разных химических элементов на Солнце — в его фотосфере, во внешних геосферах Земли, на Луне и метеоритах. Согласно господствующему представлению, распределение элементов в Солнечной системе от центра к периферии определяется их массами: под действием солнечного ветра лёгкие элементы «выдуваются» на периферию, а тяжёлые остаются в центре. Однако анализ, проведённый Лариным, показал, что это распределение зависит не от массы, а от потенциала ионизации элемента (элемент тем дальше находится от Солнца, чем этот потенциал выше), и, исходя из этого, водорода в Земле должно быть существенно больше, чем принято считать. При этом гидриды в процессе сепарации вещества Земли оказались в её центральных областях. Далее Ларин предположил, что в результате радиоактивного распада химических элементов в глубинах Земли и, возможно, под влиянием других факторов происходит высвобождение водорода из гидридов, выход его на земную поверхность — и далее в атмосферу и за её пределы.
Эту концепцию В. Н. Ларин изложил в своей докторской диссертации2 на тему «Земля: состав, строение и развитие (альтернативная глобальная концепция)», которая в 1993 году была опубликована под названием «Hydridic Earth: the New Geology of Our Primordially Hydrogenrich Planet»3 («Гидридная Земля: новая геология нашей первоначально богатой водородом планеты»). А в более популярной форме идеи Ларина изложены в его книге «Наша Земля»4.
Если концепция Ларина подтвердится, дело останется за малым — найти места выхода свободного водорода на земную поверхность. И такие выходы нашли, в ряде случаев — с высокой концентрацией водорода — во многих точках земного шара, привязанные к определённым геологическим структурам, в том числе на территории России, также в Омане, Австралии, США и других странах.
В целом в мире опубликовано порядка сотен сообщений исследователей из разных стран о нахождении выходов водорода. В большинстве случаев выходы были обнаружены случайно, как, например, в 1987 году в Мали у села Буракебугу5.
Большой вклад в исследование водородной дегазации Земли внёс также российский геолог, доктор геолого-минералогических наук Владимир Леонидович Сывороткин. Результаты своих исследований он изложил в докторской диссертации, в книге «Глубинная дегазация Земли и глобальные катастрофы»6 и в других, более поздних публикациях. Выходы водорода Сывороткин связывает прежде всего с рифтовыми зонами. Согласно его исследованиям, рифтовые зоны также совпадают с зонами отрицательных озоновых аномалий в стратосфере. Отметим, что, когда рассматриваются возможные экологические побочные эффекты водородной экономики, упоминается опасность утечек водорода из систем производства и транспортировки, в том числе, риск попадания водорода в стратосферу и разрушения озонового слоя. Согласно же исследованиям Сывороткина, периодическое разрушение озонового слоя носит природный характер — через водородную дегазацию. Владимир Леонидович, среди прочего, обращает внимание на феномен серебристых облаков — дело в том, что механизмы доставки воды на высоты, где они образуются (выше 70 км), до сих пор непонятны, а водородная дегазация и далее химическая реакция водорода с кислородом на этих высотах может дать адекватное объяснение данному явлению.
Есть предположение, что водородная дегазация свидетельствует о постоянном воспроизводстве месторождений углеводородов. Газ и нефть слагают два основных элемента — углерод и водород. И если углерода в земной коре очевидно много, то вопрос, откуда, собственно, взялся водород для формирования этих месторождений, в геологии остаётся открытым. Между тем, есть свидетельства вторичного пополнения уже исчерпанных нефтяных месторождений. Этот эффект известен и описан, в частности, для месторождений Поволжья (Алексеевское, Малышевское, Ромашкинское), Северного Кавказа, ряда месторождений в США. И если концепция водородной дегазации Земли верна, она даёт объяснение и этому феномену.
Хотя вопрос о составе глубинных слоёв Земли остаётся дискуссионным и делать однозначные выводы о возможностях добычи в промышленных масштабах свободного водорода, исходящего из глубин Земли, пока рано, имеющиеся данные обнадёживают, так что поиск свободного водорода, выходящего на земную поверхность, может иметь перспективы.
***
Потенциал ионизации элемента, или энергия его ионизации — минимальная энергия, которую необходимо затратить для отрыва электрона от атома.
Рифтовые зоны — протяжённые полосы (длиной в сотни и тысячи километров) тектонических зон, в которых происходит подъём мантийного материала. Этот подъём сопровождается распространением в стороны, что вызывает поперечное растяжение в верхних этажах земной коры. Рифтовые зоны пролегают через континенты и океаны.
Фотосфера Солнца — нижний слой его атмосферы, в котором формируется непрерывный спектр излучения Солнца в видимом диапазоне. Отметим, что у звёзд под атмосферой понимается не газовая оболочка, а её внешние слои.
Комментарии к статье
1 По данным International Energy Agency.
2 Ларин В. Н. Земля: состав, строение и развитие (альтернативная глобальная концепция): дисс. док-тора геол.-минер. наук, 1991.
3 Edited by C. Warren Hunt//Polar Publishing, Canada. 1993, 242 p.
4 Ларин В. Н. Наша земля. — М.: Агар, 2005. — 244 с.
5 Prinzhofer A., Tahara Cissé C. S., Diallo A. B. Discovery of a large accumulation of natural hydrogen in Bourakebougou (Mali) // International Journal of Hydrogen Energy, V. 43, Is. 42, 2018, pp. 19315—19326.
6 Сывороткин В. Л. Глубинная дегазация Земли и глобальные катастрофы. — М.: Геоинформцентр, 2002 (ЗАО Астра семь). — 250 с.
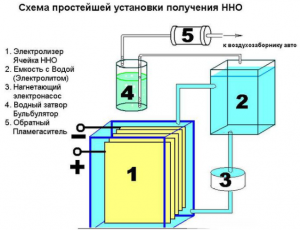
Как добыть водород в домашних условиях
Водород – первый элемент таблицы Менделеева, самое распространенное на Земле вещество. Повсеместно используется в пищевой, авиационной и химической индустрии. Это бесцветный легкий газ. В домашних условиях можно получить водород, используя реакции алюминия и цинка с водным раствором щелочей, реакции металлов с растворами кислот и при реакции электролиза в растворе солей, щелочей и кислот.
Вам понадобится
- пластиковая бутылка емкостью 1,5 литра, резиновый шарик, кастрюля с водой, гидроксид калия или гидроксид натрия (каустическая сода, едкий натр), 40 сантиметров проволоки из алюминия, кусочек цинка, стеклянная емкость с узким горлышком, раствор соляной кислоты, резиновый шарик, аккумулятор 12 Вольт, провод из меди, провод из цинка, стеклянный сосуд, вода, поваренная соль, клей, шприц.
Инструкция
Заполните наполовину водой пластиковую бутылку. Киньте в бутылку и растворите в воде 10-15 грамм едкого натра или каустической соды. Поставьте бутылку в кастрюлю с водой. Нарежьте алюминиевую проволоку кусочками по 5 сантиметров длиной и киньте в бутылку. Наденьте на горловину бутылки резиновый шарик. Выделяемый во время реакции алюминия с раствором щелочи водород будет собираться в резиновом шарике. Эта реакция происходит с бурным выделением тепла — будьте осторожны!
Налейте в стеклянную емкость соляной кислоты и киньте в нее цинк. Наденьте на горловину стеклянной емкости воздушный шарик. Выделяемый во время реакции цинка с соляной кислотой водород будет собираться в воздушном шаре.
Налейте в стеклянную емкость воду и размешайте в ней 4–5 столовых ложек поваренной соли. Затем просуньте в шприц со стороны поршня медный провод. Герметизируйте это место клеем. Опустите шприц в сосуд с соляным раствором и отодвигая поршень, заполните шприц. Подключите медный провод к отрицательному выводу аккумулятора. Опустите рядом со шприцом в раствор соли цинковый провод и подключите его к положительному выводу аккумулятора. В результате реакции электролиза около медного провода выделяется водород, который вытесняет из шприца соляной раствор, контакт медного провода с соляным раствором прервется, и реакция прекратится.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Получение водорода в промышленных и домашних условиях
Развитие водородной энергетики связано с универсальностью применения этого элемента в качестве энергоносителя, неограниченностью его запасов, экологичностью технологий и увеличением показателей качества работы энергетических систем. Главной задачей сейчас является повышение экономичности добыча водорода: пока оно дороже, чем применение природного газа в энергетике.
Содержание
- Способы получения водорода
- Добыча водорода в условиях домашнего хозяйства
- Правила техники безопасности
Способы получения водорода
Водород – газообразный элемент без цвета и запаха с плотностью 1/14 по отношению к воздуху. В свободном состоянии он встречается редко. Обычно водород соединен с другими химическими элементами: кислородом, углеродом.
Получение водорода для промышленных нужд и энергетики проводится несколькими методами. Самыми популярными считаются:
- электролиз воды;
- метод концентрирования;
- низкотемпературная конденсация;
- адсорбция.
Выделить водород можно не только из газовых или водных соединений. Добыча водорода производится при воздействии на дерево и уголь высокими температурами, а также при переработке биоотходов.
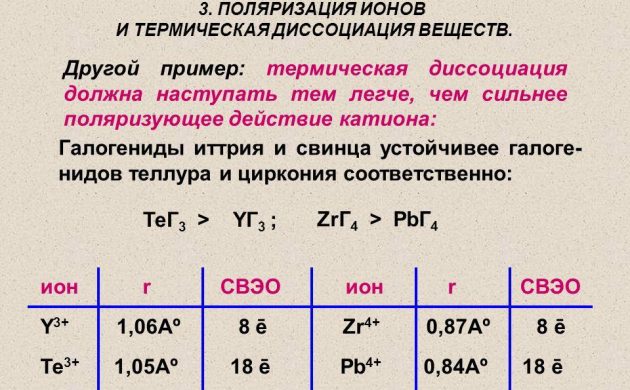
Атомный водород для энергетики получают, используя методику термической диссоциации молекулярного вещества на проволоке из платины, вольфрама либо палладия. Ее нагревают в водородной среде под давлением менее 1,33 Па. А также для получения водорода используются радиоактивные элементы.
Термическая диссоциация
Электролизный метод
Наиболее простым и популярным методом выделения водорода считается электролиз воды. Он допускает получение практически чистого водорода. Другими преимуществами этого способа считаются:
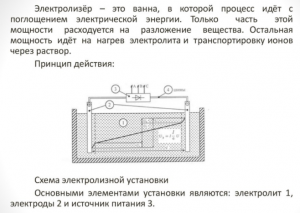
Принцип действия электролизного генератора водорода
- доступность сырья;
- получение элемента под давлением;
- возможность автоматизации процесса из-за отсутствия движущихся частей.
Процедура расщепления жидкости электролизом обратен горению водорода. Его суть в том, что под воздействием постоянного тока на электродах, опущенных в водный раствор электролита, выделяются кислород и водород.
Дополнительным преимуществом считается получение побочных продуктов, обладающих промышленной ценностью. Так, кислород в большом объеме необходим для катализации технологических процессов в энергетике, очистки почвы и водоемов, утилизации бытовых отходов. Тяжелая вода, получаемая при электролизе, в энергетике используется в атомных реакторах.
Получение водорода концентрированием
Этот способ основан на выделении элемента из содержащих его газовых смесей. Так, наибольшая часть производимого в промышленных объемах вещества, извлекается с помощью паровой конверсии метана. Добытый в этом процессе, водород используют в энергетике, в нефтеочистительной, ракетостроительной индустрии, а также для производства азотных удобрений. Процесс получения H2 осуществляют разными способами:
- короткоцикловым;
- криогенным;
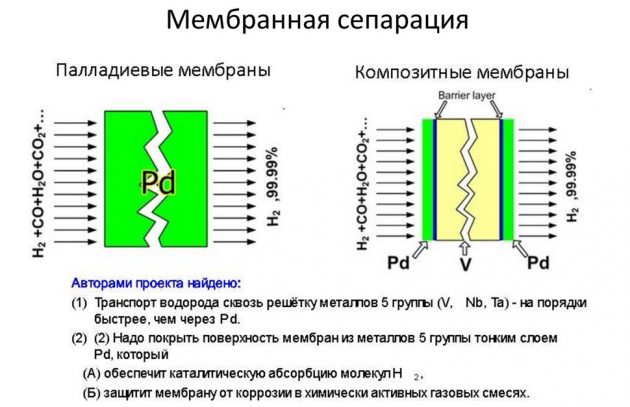
- мембранным.
Последний способ считается наиболее эффективным и менее затратным.
Конденсация под действием низких температур
Эта методика получения H2 заключается в сильном охлаждении газовых соединений под давлением. В результате они трансформируются в двухфазную систему, которая впоследствии разделяется сепаратором на жидкое составляющее и газ. Для охлаждения применяют жидкие среды:
- воду;
- сжиженный этан или пропан;
- жидкий аммиак.
Эта процедура не так проста, как кажется. Чисто разделить углеводородные газы за один раз не получится. Часть компонентов уйдет с газом, забираемым из сепарационного отсека, что не экономично. Решить проблему можно глубоким охлаждением сырья перед сепарацией. Но это требует больших энергозатрат.
В современных системах низкотемпературных конденсаторов дополнительно предусмотрены колонны деметанизации либо деэтанизации. Газовую фазу выводят с последней сепарационной ступени, а жидкость направляется в ректификационную колонну с потоком сырого газа после теплообмена.
Способ адсорбции
Во время адсорбции для выделения водорода используют адсорбенты – твердые вещества, поглощающие необходимые компоненты газовой смеси. В качестве адсорбентов применяют активированный уголь, силикатный гель, цеолиты. Для осуществления этого процесса применяют специальные аппараты – циклические адсорберы или молекулярные сита. При реализации под давлением этот метод позволяет извлекать 85-процентный водород.
Если сравнивать адсорбцию с низкотемпературной конденсацией, можно отметить меньшую материальную и эксплуатационную затратность процесса – в среднем, на 30 процентов. Методом адсорбции производят водород для энергетики и с применением растворителей. Такой способ допускает извлечение 90 процентов H2 из газовой смеси и получение конечного продукта с концентрацией водорода до 99,9%.
Добыча водорода в условиях домашнего хозяйства
Высокотемпературные методы производства водорода в домашних условиях неприменимы. Здесь чаще всего используют электролиз воды.
Выбор электролизера
Для получения элемента дома необходим специальный аппарат – электролизер. Вариантов такого оборудования на рынке много, аппараты предлагают как известные технологические корпорации, так и мелкие производители. Брендовые агрегаты дороже, но качество их сборки выше.
Домашний прибор отличается малыми габаритами и легкостью в эксплуатации. Основными деталями его являются:
Электролизер – что это
- риформер;
- система очистки;
- топливные элементы;
- компрессорное оборудование;
- емкость для хранения водорода.
В качестве сырья берется простая вода из-под крана, а электричество идет из обычной розетки. Сэкономить на электроэнергии позволяют агрегаты на солнечных батареях.
«Домашний» водород применяют в системах отопления или приготовления пищи. А также им обогащают бензовоздушную смесь, чтобы повысить мощность двигателей автомобиля.
Изготовление аппарата своими руками
Еще дешевле сделать прибор самому в домашних условиях. Сухой электролизер выглядит как герметичный контейнер, который представляет собой две электродные пластины в емкости с электролитическим раствором. Во Всемирной сети предлагаются разнообразные схемы сборки аппаратов разных моделей:
- с двумя фильтрами;
- с верхним либо нижним расположением контейнера;
- с двумя или тремя клапанами;
- с оцинкованной платой;
- на электродах.
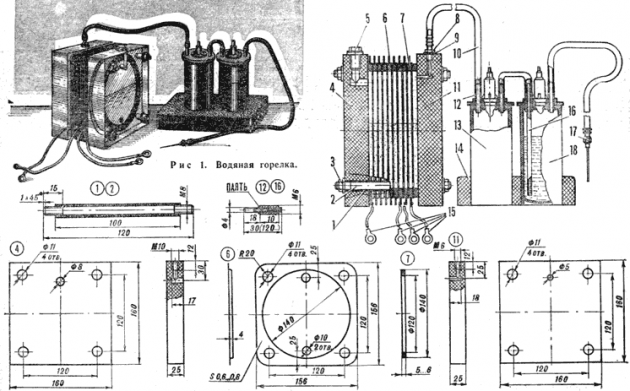
Схема устройства электролиза
Простой прибор для получения водорода создать несложно. Для него потребуются:
- листовая нержавеющая сталь;
- прозрачная трубка;
- штуцеры;
- пластиковая емкость (1,5 л);
- водяной фильтр и обратный клапан.
Устройство простого прибора для получения водорода
Помимо этого, нужны будут различные метизы: гайки, шайбы, болты. Первым делом нужно распилить лист на 16 квадратных отсеков, у каждого из них спилить угол. В противоположном от него углу требуется высверлить отверстие для болтового крепления пластин. Для обеспечения постоянного тока пластины нужно подключать по схеме: плюс–минус–плюс–минус. Изолируют эти детали друг от друга с помощью трубки, а на соединении болтом и шайбами (по три штуки между пластинками). На плюс и минус насаживают по 8 пластин.
При правильной сборке ребра пластинок не будут задевать электроды. Собранные детали опускают в емкость из пластика. В месте касания стенок болтами делают два установочных отверстия. Устанавливают защитный клапан для удаления избытка газа. В крышку контейнера монтируют штуцеры и герметизируют швы силиконом.
Тестирование аппарата
Чтобы протестировать аппарат, выполняют несколько действий:
Схема получения водорода
- Наполняют жидкостью.
- Прикрыв крышкой, соединяют один конец трубки со штуцером.
- Второй опускают в воду.
- Подключают к источнику питания.
После включения прибора в розетку через несколько секунд будет заметен процесс электролиза и выпадение осадка.
Чистая вода не обладает хорошей электропроводностью. Для улучшения этого показателя нужно создать электролитический раствор, добавив щелочь – гидроксид натрия. Он есть в составах для очищения труб наподобие «Крота».
Правила техники безопасности
Получение водорода в домашних условиях возможно лишь при ответственном подходе к работе. Этот газ способен легко загореться или взорваться, особенно при использовании аппаратов, собранных своими руками.
Чтобы избежать утечек, перед процедурой электролиза следует проверить герметичность всех частей электролизера:
Техника безопасности при работе с водородом
- трубки;
- насос;
- резервуар.
Небезопасными могут быть и покупные аппараты, особенно неизвестных производителей. Брак может случиться и у самых известных брендов, но риск этого намного меньше – там продукцию тщательно проверяют.
В промышленности добыча водорода необходима для энергетики, например, на нем работают такие энергоисточники, как высокотемпературные реакторы с гелиевым теплоносителем. Применяют элемент и в производстве пластиков, синтетических волокон, извести и цемента, листового стекла. В домашних условиях его используют для отопления помещений и снижения расходов автомобильного топлива.
Видео по теме: Водород – открытие, получение, применение
Как в недрах Земли образуется водород?
В последнее время обнаружено ряд признаков того, что в недрах Земли может содержаться большое количество водорода. Причем речь идет не просто о предположениях ученых. Ранее мы рассказывали, что в разных точках мира уже имеются несколько работающих скважин, из которых добывается водород. В ближайшее время их наверняка станет больше, так как десятки стартапов, многие из которых находятся в Австралии, борются за права на разведку этого газа. В прошлом году Американская ассоциация геологов-нефтяников сформировала свой первый комитет по природному водороду, а Геологическая служба США начала свою первую работу по выявлению перспективных зон его добычи. Даже нефтегазовые компании, такие как бразильская GEO4U, все больше начинают заниматься водородом. Но откуда вообще берется этот газ в недрах нашей планеты и действительно ли он является возобновляемым?
Водород может быть возобновляемым источником энергии, который образуется в недрах Земли
Водород в недрах Земли возобновляется?
Ранее мы рассказывали, что водород, в отличие от нефти, возобновляется. Причем, судя по всему, существует сразу несколько механизмов образования этого газа. Один из наиболее распространенных называется серпентинизацией.
В результате воздействия воды, высокой температуры и давления, минерал оливин превращается в другой вид минерала, который называется серпентинитом. В ходе этой реакции железо окисляется, захватывая атомы кислорода из молекул воды и выделяя при этом водород. Как показало исследование, проведенное в 2014 году, в результате серпентизации образуется 80% от всего водорода, возникающего внутри Земли.
Оливин — минерал, благодаря которому в недрах Земли образуется большое количество водорода
Другой механизм образования водорода называется радиолизом. Радиоактивные элементы в земной коре, такие как уран и торий, распадаются, в результате чего излучают альфа-частицы. Это излучение в свою очередь может расщеплять молекулы воды под землей и генерировать водорода.
Некоторые ученые выдвигают более радикальную версию — на поверхность земной коры просачивается первичный водород, попавший в железное ядро планеты вскоре после ее рождения. То есть он поднимается на поверхность, преодолевая тысячи километров.
Однако информации о формировании водорода пока еще не так много, поэтому ученые досконально не знают как он возникает и мигрирует. Кроме того, неизвестно, может ли водород накапливаться в достаточном количестве, чтобы его можно было использоваться для коммерческих целей. Дело в том, что в большинстве известных источников водорода слишком мало, чтобы можно было добывать газ в промышленных масштабах.
“Интерес быстро растет, но научных фактов по-прежнему не хватает” — говорит Фредерик-Виктор Донзе, геофизик, сотрудник Университета Гренобль-Альпы.
Где имеются месторождения водорода?
Ученые обнаружили множество водорода вблизи вулканического Срединно-Атлантического хребта на дне Атлантического океана. Газ в большом количестве выделяется на участке, известном как “Затерянный город”. Свое название он получил из-за возвышающихся “дымоходов” так называемых “белых курильщиков”. Из них бьет богатая минералами горячая вода.
Учены обнаружили водород на дне Атлантического океана на участке, именуемом «Затерянным городом»
В Исландии, расположенной между Срединно-Атлантическим хребтом, ученые зафиксировали сопоставимые потоки водорода в некоторых горячих источниках и геотермальных скважинах, которые находятся на разных участках страны. Об этом сообщалось в исследовании, опубликованном в прошлом году.
Отсюда следует, что водород имеется на стыке тектонических плит. Однако для коммерческих целей исследователи ищут этот в кратонах, то есть самых древних слоях земной коры, которые еще называют древними “фундаментами” континентов. Внутри них содержатся полосы богатых железом пород, которые называются зеленокаменными поясами. Они представляют собой остатки океанической коры, зажатой между плитами в результате древних столкновений континентов.
Скважину в Мали питает водород, возникающий в западноафриканском кратоне
По мнению ученых, оливин и другие минералы залегают здесь достаточно глубоко, в результате чего их температура превышает 200 градусов. В то же время на эту глубину еще просачивается вода. Как мы сказали выше, такие условия являются идеальными для образования водорода. К примеру, зеленокаменные пояса в западноафриканском кратоне стимулируют производство водорода, который вырывается на поверхность из скважины в Мали.
Обязательно переходите по этой ссылке, чтобы подписаться на наш ЯНДЕКС.ДЗЕН КАНАЛЕ. С ним вы будете в курсе самых последних событий в мире науки и высоких технологий.
Надо сказать, что по мнению ученых все вышеперечисленные версии образования водорода могут быть ошибочными. Однако для отрасли это не имеет значение. Напомним, что нефтяная промышленность возникла задолго до того, как ученые выяснили происхождение нефти. Более того, даже сейчас относительно происхождения нефти ведутся споры. Некоторые ученые считают, что нефть способна возобновляться. Поэтому в настоящее время для индустрии важно лишь одно — выяснить каковы запасы водорода, на которые можно рассчитывать.
В уроке 26 «Получение водорода и его применение» из курса «Химия для чайников» узнаем о получении водорода в лабораториях и в промышленности, а также выясним в каких отраслях промышленности его применяют.
Водород находит широкое применение в технике и лабораторных исследованиях. Мировое промышленное производство водорода из меряется десятками миллионов тонн в год.
Выбор промышленного способа получения простых веществ зависит от того, в какой форме соответствующий элемент находится в природе. Водород находится в природе преимущественно в соединениях с атомами других элементов. Поэтому для его получения необходимо использовать химические методы. Эти же методы применяют для получения водорода и в лабораторной практике.
Получение водорода в лаборатории
В лабораториях водород получают уже известным вам способом, действуя кислотами на металлы: железо, цинк и др. Поместим на дно пробирки три гранулы цинка и прильем небольшой объем соляной кислоты. Там, где кислота соприкасается с цинком (на поверхности гранул), появляются пузырьки бесцветного газа, которые быстро поднимаются к поверхности раствора:
Атомы цинка замещают атомы водорода в молекулах кислоты, в результате чего образуется простое вещество водород Н2, пузырьки которого выделяются из раствора. Для получения водорода таким способом можно использовать не только хлороводородную кислоту и цинк, но и некоторые другие кислоты и металлы.
Соберем водород методом вытеснения воздуха, располагая пробирку вверх дном (объясните почему), или методом вытеснения воды и проверим его на чистоту. Пробирку с собранным водородом наклоняем к пламени спиртовки. Глухой хлопок свидетельствует о том, что водород чистый; «лающий» громкий звук взрыва говорит о загрязненности его примесью воздуха.
В химических лабораториях для получения относительно небольших объемов водорода обычно применяют способ разложения воды с помощью электрического тока:
Из уравнения процесса разложения следует, что из 2 моль воды образуются 2 моль водорода и 1 моль кислорода. Следовательно, и соотношение объемов этих газов также равно:
Получение водорода в промышленности
Очевидно, что при огромных объемах промышленного производства сырьем для получения водорода должны быть легкодоступные и дешевые вещества. Такими веществами являются природный газ (метан СН4) и вода. Запасы природного газа очень велики, а воды — практически неограниченны.
Самый дешевый способ получения водорода — разложение метана при нагревании:
Эту реакцию проводят при температуре около 1000 °С.
В промышленности водород также получают, пропуская водяные пары над раскаленным углем:
Существуют и другие промышленные способы получения водорода.
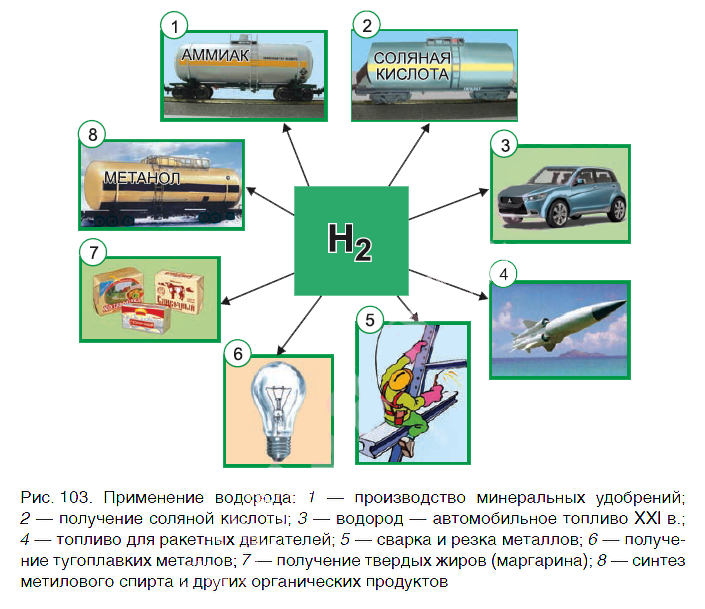
Применение водорода
Водород находит широкое практическое применение. Основные области его промышленного использования показаны на рисунке 103.
Значительная часть водорода идет на переработку нефти. Около 25 % производимого водорода расходуется на синтез аммиака NH3. Это один из важнейших продуктов химической промышленности. Производство аммиака и азотных удобрений на его основе осуществляется в нашей стране на ОАО «Гродно Азот». Республика Беларусь поставляет азотные удобрения во многие страны мира.
В большом количестве водород расходуется на получение хлороводородной кислоты. Реакция горения водорода в
кислороде используется в ракетных двигателях, выводящих в космос летательные аппараты. Водород применяют и для получения металлов из оксидов. Таким способом получают тугоплавкие металлы молибден и вольфрам.
В пищевой промышленности водород используют в производстве маргарина из растительных масел. Реакцию горения водорода в кислороде применяют для сварочных работ. Если использовать специальные горелки, то можно повысить температуру пламени до 4000 оС. При такой температуре проводят сварочные работы с самыми тугоплавкими материалами.
В настоящее время в ряде стран, в том числе и в Беларуси, начаты исследования по замене невозобновляемых источников энергии (нефти, газа, угля) на водород. При сгорании водорода в кислороде образуется экологически чистый продукт — вода. А углекислый газ, вызывающий парниковый эффект (потепление окружающей среды), не выделяется.
Предполагают, что с середины XXI в. должно быть начато серийное производство автомобилей на водороде. Широкое применение найдут домашние топливные элементы, работа которых также основана на окислении водорода кислородом.
Краткие выводы урока:
- В лаборатории водород получают действием кислот на металлы.
- В промышленности для получения водорода используют доступное и дешевое сырье — природный газ, воду.
- Водород — это перспективный источник энергии XXI в.
Надеюсь урок 26 «Получение водорода и его применение» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.