Как читать таблицы водяного пара
Если вы едете по неизвестной местности, вам понадобится карта или навигатор, если вы летите на самолете, вам не обойтись без расписания полётов. Так и таблицы водяного пара необходимы всем пользователям в индустрии пара. В этой статье мы познакомимся с таблицами пара, рассмотрим их виды и немного поговорим о присутствующих в них элементах.
Таблицы насыщенного водяного пара
Таблицы насыщенного водяного пара — необходимый инструмент для любого инженера, работающего с паром. Обычно их используют для определения зависимости температуры насыщенного пара от парового давления или, наоборот, давления от температуры насыщенного пара. Кроме этих параметров, таблицы обычно включают и другие показатели, такие как удельная энтальпия (h) и удельный объём (v).
Данные таблиц насыщенного водяного пара всегда отображают информацию о конкретной точке насыщения известной как точка кипения. Это точка, в которой вода (жидкость) и пар (газ) могут сосуществовать при одинаковых температуре и давлении. Так как H2O может быть и в жидком, и в газообразном состоянии, нам будут необходимы две подборки данных: данные о насыщенной воде (жидкости), которые обычно обозначаются подстрочной буквой f, и данные о насыщенном паре (газе), которые обозначают подстрочной буквой g.
Пример таблицы насыщенного пара
Обозначения:
- P = Давление пара/воды
- T = Точка насыщения пара/воды (точка кипения)
- vf = Удельный объём насыщенной воды (жидкости)
- vg = Удельный объём насыщенного пара (газа)
- hf = Удельная энтальпия насыщенной воды (энергия, необходимая для подогрева воды от 0 °C до точки кипения)
- hfg = Скрытое тепло испарения (энергия, необходимая для трансформации насыщенной воды в насыщенный пар)
- hg = Удельная энтальпия насыщенного пара (энергия, необходимая для получения пара из воды с температурой 0 °C)
* Источник: 1999 таблицы пара Японского общества инженеров-механиков
При нагреве обычно используется скрытое тепло испарения (Hfg). Как видно из таблицы, это скрытое тепло испарения будет выше при более низком давлении. По мере увеличения парового давления скрытое тепло постепенно снижается и достигает 0 при суперкритическом давлении, например, 22.06 МПа.
Полезно знать
Два формата: на основе давления и температуры
Так как давление и температура насыщенного пара напрямую связаны друг с другом, таблицы пара обычно доступны в двух форматах: на основе давления и температуры. В обоих содержится одинаковая информация, но классифицирована она по-разному.
Таблица насыщенного водяного пара, основанная на давлении
| Давл. (изб.) | Темп. | Удельный объём | Удельная энтальпия | |||
|---|---|---|---|---|---|---|
| кПа изб. | °C | м3/кг | кДж/кг | |||
| P | T | Vf | Vg | Hf | Hfg | Hg |
| 0 | 99.97 | 0.0010434 | 1.673 | 419.0 | 2257 | 2676 |
| 20 | 105.10 | 0.0010475 | 1.414 | 440.6 | 2243 | 2684 |
| 50 | 111.61 | 0.0010529 | 1.150 | 468.2 | 2225 | 2694 |
| 100 | 120.42 | 0.0010607 | 0.8803 | 505.6 | 2201 | 2707 |
Таблица насыщенного водяного пара, основанная на температуре
| Темп. | Давл. (изб.) | Удельный объём | Удельная энтальпия | |||
|---|---|---|---|---|---|---|
| °C | кПа изб. | м3/кг | кДж/кг | |||
| T | P | Vf | Vg | Hf | Hfg | Hg |
| 100 | 0.093 | 0.0010435 | 1.672 | 419.1 | 2256 | 2676 |
| 110 | 42.051 | 0.0010516 | 1.209 | 461.4 | 2230 | 2691 |
| 120 | 97.340 | 0.0010603 | 0.8913 | 503.8 | 2202 | 2706 |
| 130 | 168.93 | 0.0010697 | 0.6681 | 546.4 | 2174 | 2720 |
| 140 | 260.18 | 0.0010798 | 0.5085 | 589.2 | 2144 | 2733 |
| 150 | 374.78 | 0.0010905 | 0.39250 | 632.3 | 2114 | 2746 |
Разные единицы измерения: избыточное и абсолютное давление
Таблицы насыщенного пара также используют два различных вида давления: абсолютное и манометрическое (избыточное).
- Абсолютное давление — это нулевая точка по отношению к абсолютному вакууму.
- Манометрическое давление — это нулевая точка по отношению к атмосферному давлению (101.3 кПа).
Таблица насыщенного пара с абсолютным давлением
| Давл. (абс.) | Темп. | Удельный объём | Удельная энтальпия | |||
|---|---|---|---|---|---|---|
| кПа | °C | м3/кг | кДж/кг | |||
| P | T | Vf | Vg | Hf | Hfg | Hg |
| 0 | — | — | — | — | — | — |
| 20 | 60.06 | 0.0010103 | 7.648 | 251.4 | 2358 | 2609 |
| 50 | 81.32 | 0.0010299 | 3.240 | 340.5 | 2305 | 2645 |
| 100 | 99.61 | 0.0010432 | 1.694 | 417.4 | 2258 | 2675 |
Таблица насыщенного пара с избыточным давлением
| Давл. (изб.) | Темп. | Удельный объём | Удельная энтальпия | |||
|---|---|---|---|---|---|---|
| кПа изб. | °C | м3/кг | кДж/кг | |||
| P | T | Vf | Vg | Hf | Hfg | Hg |
| 0 | 99.97 | 0.0010434 | 1.673 | 419.0 | 2257 | 2676 |
| 20 | 105.10 | 0.0010475 | 1.414 | 440.6 | 2243 | 2684 |
| 50 | 111.61 | 0.0010529 | 1.150 | 468.2 | 2225 | 2694 |
| 100 | 120.42 | 0.0010607 | 0.8803 | 505.6 | 2201 | 2707 |
Избыточное давление было придумано для простоты измерения давления по отношению к тому, которое мы обычно испытываем.
В таблицах пара, составленных на основе манометрического давления, атмосферное давление определяется как 0, а в таблицах с абсолютным давлением — 101.3 кПа. А для того чтобы отличать избыточное давление от абсолютного в конце добавляют «изб.», например, кПа изб. или фт/кв. дюйм изб..
Перевести показатели избыточного давления в показатели абсолютного
Для единиц СИ
Давление пара [кПа изб.] = Давление пара [кПа изб.] + 101.3 кПа
Важное замечание: Проблемы могут возникнуть в том случае, если перепутать абсолютное и манометрическое давление, именно поэтому надо быть особенно внимательными с единицами давления, указанными в таблице.
Сводная таблица
Избыточное давление
- Нулевая точка отсчёта при атмосферном давлении*
- Нулевое давление = Атмосферное давление
Абсолютное давление:
- Нулевая точка отсчёта при атмосферном давлении
- Нулевое давление = Абсолютный вакуум
*Атмосферное давление — 101.3 кПа
Таблицы перенасыщенного пара
Информацию о перенасыщенном паре нельзя получить из обычных таблиц насыщенного пара, для этого существуют специальные таблицы перенасыщенного пара. Происходит это потому, что температура перенасыщенного пара в отличии от температуры насыщенного может существенно меняться при одном и том же давлении.
В действительности, количество возможных комбинаций температуры и давления настолько велико, что даже теоретически не представляется возможным собрать их в одной таблице. В результате для перегретого пара используется общая сводная таблица данных о температуре и давлении.
Пример таблицы перенасыщенного пара
В приведенной выше таблице есть данные об удельном объёме (Vg), удельной энтальпии (Hg) и удельном тепле (Sg) при типичных значениях давления и температуры.
Калькулятор определяет параметры насыщенного водяного пара по заданному давлению пара. На основании выбранных параметров насыщенного пара определяются:
-
- температура насыщенного пара (по табличным данным) на линии насыщения;
- плотность насыщенного пара (по табличным данным) на линии насыщения;
- удельная теплота парообразования/удельная энтальпия насыщенного пара (по табличным данным) на линии насыщения;
- удельный объем насыщенного водяного пара (расчет) на линии насыщения;
- удельный объем насыщенного водяного пара (расчет) с учетом степени сухости пара;
- удельная энтальпия воды (расчет) на линии насыщения;
- удельная энтальпия насыщенного пара (расчет) с учетом степени сухости пара;
- масса пара в трубопроводе (расчет);
- масса пара в сосуде/оборудовании (расчет);
- скорость пара в трубопроводе (расчет);
- рекомендуемая скорость пара в трубопроводе (справочные данные).
Определение свойств насыщенного пара.
Определение параметров инженерных систем исходя из выбранных свойств насыщенного пара.
Для выполнения расчета необходимо задать исходные данные выше.
Примечание.
Расчет составлена на базе справочных данных («Таблицы теплофизических свойств воды и водяного пара», Издательство МЭИ, 1999 г.) приведенных в табличном виде.
Степень сухости пара – массовая доля сухого насыщенного пара в влажном. Обычно сухость пара обозначается буквой — Х. Безразмерная величина. Данная величина может быть отрицательной для недогретой до кипения воды и превосходить единицу для перегретого пара. Для насыщенного пара находится в пределах от 0 до 1. При степени сухости насыщенного пара Х=1 пар называют сухой насыщенный пар (СНП). При степени сухости насыщенного пара от 0 до 1 пар называют влажный насыщенный пар.
При эксплуатации паровых котлов, паропроводов, турбин, машини и т.д. стремятся к получению и использованию СНП. Повышение влажности пара (y, y=(1-x)), ведет к увеличению эксплуатационных затрат.
В комментарии к калькулятору приветствуются пожелания, замечания и рекомендации по улучшению программы.
Поделиться ссылкой:

Таблицы DPVA.ru — Инженерный Справочник
Адрес этой страницы (вложенность) в справочнике dpva.ru: 
Свойства насыщенного водяного пара от 0 до 100 бар. Вариант для печати.Давление насыщенного пара. Температура кипения (конденсации). Плотность. Объемная масса (обратная плотность). Удельная энтальпия жидкой воды. Удельная энтальпия пара. Удельная теплота парообразования (конденсации). Теплоемкость пара. Динамическая вязкость пара.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Поиск в инженерном справочнике DPVA. Введите свой запрос: |
Поиск в инженерном справочнике DPVA. Введите свой запрос:
Если Вы не обнаружили себя в списке поставщиков, заметили ошибку, или у Вас есть дополнительные численные данные для коллег по теме, сообщите , пожалуйста.
Вложите в письмо ссылку на страницу с ошибкой, пожалуйста.
Коды баннеров проекта DPVA.ru
Начинка: KJR Publisiers
Консультации и техническая
поддержка сайта: Zavarka Team
Free xml sitemap generator
5.5.1. Энтальпия жидкости и пара
Напишем уравнение
первого закона термодинамики для 1 кг
тела в общем виде:
(5.6)
q=
(и2
– и1)
+ Аl
ккал/кг.
Подведенное к телу
количество теплоты затрачивается на
изменение внутренней энергии и на
совершение работы. А – коэффициент.
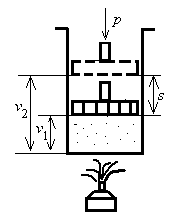
Для изобарного
процесса можно записать l
= p(v2
–v1)
(см. рис. 4.7).
Допустим, что 1 кг
газа, имеющего удельный объем v1,
заключен в цилиндр с поршнем, нагруженным
грузом.
Если этот газ
подогреть, не изменяя давления, то объем
его, очевидно, увеличиться и в какой-нибудь
момент станет равным v2.
При расширении газ произведет внешнюю
работу, которая выразится в поднятии
поршня. Как известно, работа равна
произведению силы на путь т.е.
Рис. 5.7. К объяснению
значения совершаемой работы
l
= Q∙S,
где:
l
– работа 1 кг газа при поднятии поршня
с постоянным грузом;
Q
– общее давление на поршень;
S
– расстояние,
на которое передвинулся поршень при
совершении газом работы l.
Если обозначим
давление газа, приходящегося на 1 м2
площади поршня, через р,
а площадь поршня через F
м2,
то общее давление Q
на поршень будет равно pF.
При этом l
= p·F·S
кгм/кг.
Но F·S
– объем цилиндра, имеющего площадь
основания F
и высоту S.
Обозначим этот объем через v
(удельный объем газа).
Тогда
l
= p·F·S = pv.
Как видно из рис.
4.7, v=
v2
–v1,
а поэтому
l
= p(v2
–v1)
кгм/кг.
Тогда уравнение
4.6 можно записать
q=
(и2
– и1)
+ А p(v2
–v1)
ккал/кг.
Перегруппировывая
члены в правой части уравнения, получим
(5.7)
q=
(и2
+ А pv2)
– (и1
+ А pv1)
ккал/кг.
Правая часть этого
уравнения является разностью двух
выражений, представляющих собой одну
и ту же величину вида и
+ А pv.
Эта величина называется э н т а л ь п и
е й (теплосодержанием) и обозначается
через i.
Итак,
i
(5.8)
= и +
А p
v.
Как видим, энтальпия
определяется тремя величинами: и,
р и v,
являющимися параметрами состояния
рабочего тела. Следовательно, энтальпия
тоже является параметром состояния и
должна измеряться так же, как измеряются
и
и А pv,
т.е. в килокалориях или килоджоулях. Все
величины, входящие в уравнение (4.8),
должны относится к одному состоянию
тела. Например, если состояние его
определяется точкой 1, то i1
= и1
+ А pv1
ккал/кг.
В дальнейшем мы
увидим, что энтальпия позволяет
значительно упрощать и сокращать
расчеты, связанные с теплотой, вследствие
чего этот параметр широко применяется
в теплотехнических расчетах, в особенности
в расчетах, относящихся к парам.
Если в уравнении
(4.7) для изобарного процесса подставить
величину i,
то оно приобретает очень простой вид:
(5.9)
q
= i2
– i1
ккал/кг.
Значения i
берутся из специальных таблиц или
диаграмм, о которых будет сказано ниже.
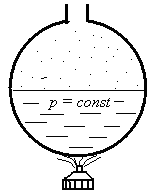
Посмотрим, как
вычисляют энтальпию для воды и пара
(см. рис. 5.8).
Рис. 5.8. К объяснению
определения энтальпии воды и пара
При нагревании
воды от 0о
С до температуры насыщения ts
вода приобретает энтальпию
,
называемой энтальпией кипящей жидкости.
После чего начинается парообразование
и получается влажный насыщенный пар,
энтальпию которого можно определить
по формуле
ккал/кг.
При этом температура
насыщения в сосуде остается постоянной,
соответствующей давлению в сосуде.
Парообразование происходит за счет
величины r,
называемой скрытой теплотой парообразования
(см. ранее). Когда вся вода испарится,
получается сухой насыщенный пар, степень
сухости которого х
равна 1. Энтальпия сухого насыщенного
пара определится как:
ккал/кг.
Нагревая далее
сухой насыщенный пар и, повышая его
температуру, получаем перегретый пар,
энтальпию которого можно определить
по формуле
ккал/кг,
где t
– температура
перегретого пара.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Насыщенный пар — это одно из самых распространенных агрегатных состояний воды, используемое в быту и промышленности.
Рассмотрим основные характеристики этого вещества, приведем таблицы свойств и основных характеристик насыщенного пара.
Содержание
- Какова важнейшая характеристика?
- Таблица
- Параметры
- Упругость
- Температура
- Влажность
- Молярная масса
- Плотность
- Давление
- Энтропия
- Энтальпия
- Применение знаний на практике
- Видео по теме статьи
- Заключение
Какова важнейшая характеристика?
Самым важным свойством насыщенного пара является термодинамическое равновесие со своей жидкостью (например, водой).
Равновесие определяет баланс температуры и влажности. Эталонным значением является вытеснение с поверхности воды, площадью 1 см2 молекул, в количестве 1022. При этом скорость испарения определяется за 1 секунду времени.
Параметр насыщения молекулами воды является основным. При низком насыщении, пар переходит в состояние сухого, а при последующем увеличении температуры, происходит его перегрев. При обычном насыщении, пар снова меняет свое агрегатное состояние во время процесса конденсации (переход из газа в жидкое состояние).
Таблица
Характеристики насыщенного пара сильно зависят от атмосферного давления и температуры. Ниже приведена таблица основных свойств:
| Температура | Давление | Энтальпия жидкости | Энтальпия пара | Объем пара | Удельная теплота образования пара | Плотность |
| 0 | 0,006 | 0 | 2493 | 206 | 2493 | 0,004 |
| 10 | 0,01 | 41 | 2512 | 106 | 2470 | 0,009 |
| 20 | 0,02 | 83 | 2532 | 57 | 2448 | 0,017 |
| 30 | 0,04 | 125 | 2551 | 32 | 2425 | 0,03 |
| 40 | 0,07 | 167 | 2570 | 19 | 2403 | 0,05 |
| 50 | 0,12 | 209 | 2589 | 12 | 2380 | 0,08 |
| 60 | 0,2 | 251 | 2608 | 7 | 2356 | 0,13 |
| 70 | 0,3 | 293 | 2626 | 5 | 2333 | 0,19 |
| 80 | 0,4 | 335 | 2644 | 3 | 2310 | 0,29 |
| 90 | 0,7 | 377 | 2662 | 2 | 2285 | 0,42 |
| 100 | 1,03 | 419 | 2679 | 1,6 | 2260 | 0,5 |
| 374 | 225 | 2100 | 2100 | 0,003 | 0 | 322 |
В таблице приведены следующие характеристики:
Температура. Указана в градусах Цельсия (°С).
- Абсолютное давление кгс/см2. В таблице прослеживается рост давления при подводе тепла.
- Энтальпия жидкости кДж/кг. Увеличивается с ростом давления и температуры.
- Энтальпия пара кДж/кг. Также рост значений при подводе тепла.
- Объем пара м3/кг. Удельный объем газа снижается при росте давления и температуры.
- Удельная теплота парообразования кДж/кг. Также уменьшается по причине снижения необходимого количества тепловой энергии для смены агрегатного состояния.
- Плотность кг/м3. При увеличении подвода тепла и давления, плотность пара увеличивается.
Исключением в таблице является температурное значение +374 градуса. Это критический температурный порог, при котором удельная теплота парообразования равна 0 при давлении 225 Па.
Параметры
На процесс образования влияют несколько основных параметров, описание которым будет дано далее.
Упругость
Упругостью насыщенного пара является значение давления, при котором возникает термодинамическое равновесие пара с жидкостью. В замкнутом пространстве и происходит процесс испарения. Упругость является парциальным давлением, отличным от атмосферного.
Температура
Это показатель, при котором происходит образование и конденсация насыщенного пара. Для воды температура образования пара варьируется от +1 до 374 градусов. Подобный пар также может образовываться с поверхности льда при температуре от 0 градусов.
Температуре насыщенного пара свойственно равновесие со своей жидкостью: при температуре кипения воды 100 градусов, этому же значению равна температура пара.
Влажность
Влажность определяется количеством молекул воды, находящихся в паре. Это значение пропорционально равно парциальному давлению пара. Для насыщенного пара влажность всегда составляет 100% из-за наличия конденсации и термодинамического равновесия.
Молярная масса
Данное значение определяет соотношение количества вещества к его массе. Единицей измерения является г/моль. Молярной массой насыщенного пара является значение 18 г/моль.
Как находить молярную массу насыщенного пара? Для вычисления этого значения используется формула:
Выражение состоит из:
- «M» — молярная масса;
- «m» — масса вещества (пара);
- «v» — количество вещества.
Ниже приведена таблица массы пара по отношению к давлению и температуре.
| Температура °С | Давление кПа | Масса г/м3 |
| 0 | 0,6 | 3,2 |
| 10 | 1,2 | 9,4 |
| 20 | 2,3 | 17,3 |
| 30 | 4,2 | 30,3 |
| 40 | 7,3 | 51 |
| 50 | 12,3 | 83 |
| 60 | 19,9 | 130 |
| 70 | 31 | 198 |
| 80 | 47 | 293 |
| 90 | 70 | 424 |
| 100 | 101 | 589 |
В данной таблице указана плотность вещества относительно давления и температуры. Плотность также рассчитывается по молярной массе:
Где:
- «M» — масса;
- «v» — объем;
- «p» — плотность.
Молярная масса насыщенного пара большого объема более точно рассчитывать по плотности газа.
Плотность
Плотность определяет, какое количество вещества покинуло жидкость в виде пара. Данное значение прямо зависит от температуры и не зависит от объема.
При повышении температуры плотность пара растет, так как все больше молекул воды покидает жидкость. Данный параметр уравновешивается при стабильном подводе тепла.
Давление
Данное значение определяет состояние пара в виде равновесного, по отношению к температуре. Давление прямо зависит от температуры. Чем выше подвод тепла к жидкости, тем быстрее происходит процесс парообразования, а значит большее количество молекул воды выходит с поверхности и насыщает пространство.
Давление стабилизируется при заданной температуре только на момент конденсации. Температура также имеет зависимость от давления. Чем оно выше, тем больше тепловой энергии требуется для испарения.
Энтропия
Энтропия по своей сути очень сложное явление. Простыми словами, энтропия пара, это некоторое количество энергии, которое тратится безвозвратно. Например, при нагреве воды от 0 до 100 градусов, часть тепловой энергии для парообразования уходит на обогрев самой емкости, окружающей среды, самого образованного пара.
Также энтропией является величина энергии при конденсации, которая расходуется на термодинамическое равновесие с жидкостью и средой.
Энтальпия
Энтальпией насыщенного пара является значение тепловой энергии, требуемой для образования пара массой 1 кг из 1 кг воды. Данное значение также зависит от температуры и давления. Таблица зависимости приведена ниже:
| Температура | Давление | Энтальпия воды | Энтальпия пара |
| 0 | 0,006 | 0 | 2493 |
| 10 | 0,01 | 41 | 2512 |
| 20 | 0,02 | 81 | 2532 |
| 30 | 0,04 | 125 | 2551 |
| 40 | 0,07 | 167 | 2570 |
| 50 | 0,12 | 209 | 2589 |
| 60 | 0,2 | 251 | 2608 |
| 70 | 0,3 | 293 | 2626 |
| 80 | 0,4 | 335 | 2644 |
| 90 | 0,7 | 377 | 2662 |
| 100 | 1,02 | 419 | 2679 |
Согласно таблице, видна зависимость потребления тепловой энергии при росте температуры. Чем выше температура среды и давление, тем выше теплосодержание как самой воды, так и ее насыщенного пара. Энтальпия насыщенного пара выражается в ккал/кг или кДж/кг.
Применение знаний на практике
Свойства насыщенного пара используются в быту и промышленности:
Энергетика использует этот тип пара для работы паровых турбин, вращающих электрические генераторы.
- Теплоэнергетика применяет в теплоносителях для отопления, размораживания или увеличения влажности.
- В быту подобный пар используется в кулинарии. Например, его можно встретить при кипячении воды в чайнике, при работе мультиварок или печей.
Подобный пар также применяется для очистки оборудования на нефтяных, газовых и химических предприятиях. Также свойства насыщенного пара используется метеорологами для расчета влажности воздуха и степени испарения естественных водных источников.
Видео по теме статьи
О насыщенном паре и его свойствах расскажет видео:
Заключение
Насыщенный пар имеет большое значение для промышленности. Расчет его свойств и характеристик помогает спроектировать новое оборудование и поддерживать его работоспособность.




 Температура. Указана в градусах Цельсия (°С).
Температура. Указана в градусах Цельсия (°С).



 Энергетика использует этот тип пара для работы паровых турбин, вращающих электрические генераторы.
Энергетика использует этот тип пара для работы паровых турбин, вращающих электрические генераторы.